Citarabina
Citarabina o citosina arabinoside è un agente chemioterapico antineoplastico utilizzato principalmente nel trattamento dei tumori delle cellule bianche del sangue, come ad esempio la leucemia mieloide acuta (LMA) e il linfoma di Hodgkin e non-Hodgkin. Il composto è noto anche come Ara-C (Arabinofuranosil citidina).[1]
Il farmaco comporta la distruzione delle cellule tumorali per un meccanismo di interferenza con la sintesi del DNA.
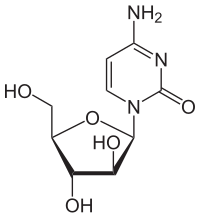
Il nome citosina arabinoside deriva dalla composizione chimica della molecola che unisce una base azotata (la citosina) con uno zucchero (l'arabinosio). La citosina normalmente si lega ad uno zucchero differente, il desossiribosio, per formare la deossicitidina, un componente chimico della molecola di DNA.
Alcune spugne usano lo zucchero arabinosio per formare dei composti diversi, che non fanno parte della molecola di DNA. Il composto fu scoperto per la prima volta proprio grazie allo studio di alcune di queste spugne.
Citosina arabinoside è chimicamente abbastanza simile alla citosina desossiribosio umana (deossicitidina) da essere incorporata nel DNA umano. Ciò però altera la trascrizione del DNA e comporta la morte cellulare.
Citarabina è stato il primo di una serie di farmaci antineoplastici (attivi contro il cancro) che si basano su una alterazione della componente zucchero dei nucleosidi. Altri farmaci antineoplastici si basano invece su modifiche interessanti la base azotata.
| Citarabina | |
|---|---|
 | |
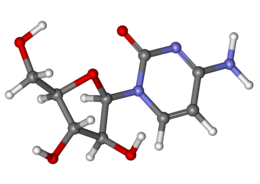 | |
| Nome IUPAC | |
| 4-ammino-1-[(2R,3S,4R,5R)-3,4-diidrossi-5-(idrossimetil)ossolan-2-il]pirimidin-2-one | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C9H13N3O5 |
| Massa molecolare (u) | 243,217 g/mol |
| Numero CAS | |
| Numero EINECS | 205-705-9 |
| Codice ATC | L01 |
| PubChem | 6253 |
| DrugBank | DBDB00987 |
| SMILES | C1=CN(C(=O)N=C1N)C2C(C(C(O2)CO)O)O |
| Dati farmacologici | |
| Modalità di somministrazione | endovenosa, intratecale, sottocutanea |
| Dati farmacocinetici | |
| Biodisponibilità | 20% orale |
| Metabolismo | Epatico |
| Emivita | bifasica: 10 min, 1-3 ore |
| Escrezione | Renale |
| Indicazioni di sicurezza | |
Storia
modificaCitarabina fu sintetizzata nel 1959 da Richard Walwick, Walden Roberts, e Charles Dekker presso l'Università della California, a Berkeley.[2] Il farmaco è stato approvato dalla Food and Drug Administration nel giugno del 1969, ed è stato inizialmente commercializzato negli Stati Uniti da Upjohn con il nome commerciale Cytosar-U.
Farmacodinamica
modificaCitosina arabinoside interferisce con la sintesi del DNA. Si tratta di un agente antimetabolita analogo delle pirimidine con il nome chimico di 1β-arabinofuranosilcitosina. La molecola si differenzia dai normali nucleotidi (citidina e deossicitidina), in quanto il ribosio ed il deossiribosio sono stati sostituiti con l'arabinosio. Una volta penetrato all'interno della cellula il composto viene rapidamente trasformato in citosina arabinoside trifosfato (ara-CTP), il metabolita attivo e responsabile del meccanismo d'azione.
Ara-CTP sembra in grado di inibire la sintesi del DNA quando la cellula si trova in una specifica fase del ciclo cellulare, ovvero nella fase S dell'interfase, la fase di sintesi del DNA.
Ne consegue che le cellule in rapida divisione, che richiedono la replicazione del DNA per mitosi, sono pertanto più sensibili al composto e perciò più colpite.[3][4]
Probabilmente la citotossicità del farmaco è in parte dovuta alla sua incorporazione nelle molecole di DNA e di RNA. Inoltre in determinate condizioni la molecola sembra inibire il passaggio delle cellule dalla fase G1 alla fase S.
Citosina arabinoside inibisce sia il DNA che la RNA polimerasi e gli enzimi nucleotidi reduttasi, necessari per la sintesi del DNA.
Quando viene utilizzato come farmaco antivirale, citarabina agisce inibendo l'utilizzo della deossicitidina. Citarabina viene rapidamente inattivata attraverso una reazione di deaminazione operata dall'enzima pirimidina-nucleoside-deaminasi e trasformata in un derivato uracilico inattivo e privo di citotossicità.
Farmacocinetica
modificaCitarabina dopo somministrazione per via orale viene rapidamente metabolizzata ed è scarsamente assorbita dal tratto gastrointestinale risultando pertanto non efficace. L'infusione continua per via endovenosa permette di ottenere livelli plasmatici relativamente costanti ed efficaci. Studi sperimentali hanno evidenziato che nell'arco di 24 ore, circa l'80% del farmaco somministrato endovena viene eliminato dall'organismo attraverso l'emuntorio renale per il 50% circa sotto forma di ara-U. La somministrazione per via intramuscolare o sottocutanea di citarabina comporta il raggiungimento di livelli plasmatici di picco entro 30-60 minuti dall'iniezione, ma comunque considerevolmente inferiori a quelli ottenibili dopo somministrazione endovenosa.
Usi clinici
modificaCitarabina trova indicazione, quasi esclusivamente in associazione con altri farmaci, principalmente nel trattamento della leucemia mieloide acuta (LMA),[5][6][7] della leucemia linfocitica acuta (LLA)[8][9] e dei linfomi, Hodgkin[10][11][12] e non-Hodgkin.[13][14][15]
Il farmaco è anche dotato di attività antivirale, ed è stato utilizzato nel trattamento dell'infezione da herpesvirus generalizzata. Tuttavia la molecola è dotata anche di importante attività immunosoppressiva comportando numerosi effetti indesiderati. Segnalazioni circa la sua inefficacia nel trattamento di diverse infezioni virali[16][17][18][19] ed il suo profilo di tossicità la rendono scarsamente utile nel trattamento delle infezioni virali nell'uomo[20] e fanno sì che venga principalmente utilizzata nella chemioterapia dei tumori ematologici.
Citarabina è utilizzata anche nello studio del sistema nervoso in quanto permette il controllo della proliferazione delle cellule gliali nelle colture.
Effetti collaterali ed indesiderati
modificaCitarabina determina mieloinibizione pertanto fra i più frequenti effetti avversi sono stati segnalati anemia, leucopenia, trombocitopenia, reticolocitopenia ed altre alterazioni a carico della popolazione cellulare del midollo osseo.
Sono inoltre possibili numerose complicanze di tipo infettivo comprendenti svariati tipi di infezioni virali, batteriche, micotiche, parassitarie in qualsiasi sede corporea. Queste infezioni sono prevalentemente lievi, ma talvolta anche gravi ed addirittura ad esito mortale.
Tra gli eventi avversi che si manifestano con notevole frequenza sono degni di menzione la nausea, l'anoressia, il vomito, la diarrea, le ulcerazioni del cavo orale ed anali, l'alterazione della funzionalità epatica, la febbre, la comparsa di rash cutaneo e di tromboflebiti.
Più raramente può comparire pericardite,[21] rabdomiolisi,[22] alterazione della funzionalità renale, esofagite, polmonite, mielopatia, neuropatia[23] e sepsi.
Una forma peculiare di tossicità da citarabina è rappresentata dalla tossicità cerebellare, specialmente nei soggetti trattati con alti dosaggi, che può portare alla atassia ed a disartria.[24][25][26][27]
Singolare anche la possibilità che, in genere nel giro di 6-12 ore dalla somministrazione, si manifesti una sindrome da citarabina, caratterizzata dalla comparsa di malessere generale, dolore muscolare ed osseo, talvolta dolore toracico, febbre, rash maculopapulare, congiuntivite. Il trattamento e la prevenzione di questa sindrome si giovano della somministrazione di farmaci corticosteroidei.[28][29][30][31]
Note
modifica- ^ H. Ogbomo, M. Michaelis; D. Klassert; HW. Doerr; J. Cinatl, Resistance to cytarabine induces the up-regulation of NKG2D ligands and enhances natural killer cell lysis of leukemic cells., in Neoplasia, vol. 10, n. 12, Dic 2008, pp. 1402-10, PMID 19048119.
- ^ Sneader, Walter, Drug discovery: a history, New York, Wiley, 2005, p. 258, ISBN 0-471-89979-8.
- ^ L. Campio, [Recent acquisitions in the metabolism, mechanism of action and toxicity of cytarabine]., in Minerva Med, vol. 62, n. 25, Mar 1971, pp. 1319-32, PMID 5552474.
- ^ S. Eridani, [Cytarabine: mechanism of action and clinical application]., in Haematologica, vol. 57, n. 7, 1972, pp. 341-58, PMID 4628582.
- ^ FR. Jack, GP. Summerfield, Long term remission of acute myeloid leukaemia with trilineage myelodysplasia treated solely with low dose cytarabine., in Clin Lab Haematol, vol. 16, n. 2, Giu 1994, pp. 197-200, PMID 7955930.
- ^ M. Low, D. Lee; J. Coutsouvelis; S. Patil; S. Opat; P. Walker; A. Schwarer; H. Salem; S. Avery; A. Spencer; A. Wei, High-dose cytarabine (24 g/m2) in combination with idarubicin (HiDAC-3) results in high first-cycle response with limited gastrointestinal toxicity in adult acute myeloid leukaemia., in Intern Med J, vol. 43, n. 3, Mar 2013, pp. 294-7, DOI:10.1111/j.1445-5994.2012.02868.x, PMID 22757980.
- ^ SX. Qian, JY. Li; HX. Wu; H. Lu; HX. Qiu; LJ. Chen; RN. Lu; W. Xu; RL. Sheng, [Standard-dose of idarubicin in combination with continuous infusion of cytarabine as induction therapy in patients with acute myeloid leukaemia]., in Zhongguo Shi Yan Xue Ye Xue Za Zhi, vol. 17, n. 1, Feb 2009, pp. 209-13, PMID 19236781.
- ^ AS. Advani, HM. Gundacker; O. Sala-Torra; JP. Radich; R. Lai; ML. Slovak; JE. Lancet; SE. Coutre; RK. Stuart; MP. Mims; PJ. Stiff, Southwest Oncology Group Study S0530: a phase 2 trial of clofarabine and cytarabine for relapsed or refractory acute lymphocytic leukaemia., in Br J Haematol, vol. 151, n. 5, Dic 2010, pp. 430-4, PMID 21113977.
- ^ AS. Boyd, Histiocyte-rich dermatoses in two patients with acute lymphocytic leukaemia treated with cytarabine., in Histopathology, vol. 45, n. 2, Ago 2004, pp. 194-6, DOI:10.1111/j.1365-2559.2004.01855.x, PMID 15279640.
- ^ J. Kuruvilla, T. Nagy; M. Pintilie; R. Tsang; A. Keating; M. Crump, Similar response rates and superior early progression-free survival with gemcitabine, dexamethasone, and cisplatin salvage therapy compared with carmustine, etoposide, cytarabine, and melphalan salvage therapy prior to autologous stem cell transplantation for recurrent or refractory Hodgkin lymphoma., in Cancer, vol. 106, n. 2, Gen 2006, pp. 353-60, DOI:10.1002/cncr.21587, PMID 16329112.
- ^ J. McCarthy, AK. Gopal, Successful use of full-dose dexamethasone, high-dose cytarabine, and cisplatin as part of initial therapy in non-hodgkin and hodgkin lymphoma with severe hepatic dysfunction., in Clin Lymphoma Myeloma, vol. 9, n. 2, Apr 2009, pp. 167-70, DOI:10.3816/CLM.2009.n.039, PMID 19406729.
- ^ R. Sinha, PJ. Shenoy; N. King; MJ. Lechowicz; K. Bumpers; D. Hutcherson; M. Arellano; A. Langston; J. Kaufman; LT. Heffner; EK. Waller, Vinorelbine, Paclitaxel, Etoposide, Cisplatin, and Cytarabine (VTEPA) Is an Effective Second Salvage Therapy for Relapsed/Refractory Hodgkin Lymphoma., in Clin Lymphoma Myeloma Leuk, Ott 2013, DOI:10.1016/j.clml.2013.05.007, PMID 24094894.
- ^ K. Merk, K. Ideström; B. Johansson; E. Kimby; C. Lindemalm; E. Osby; M. Björkholm, Mitoxantrone, etoposide, cytarabine and prednisone as salvage therapy for refractory non-Hodgkin lymphoma (NHL) and alternated with CHOP in previously untreated patients with NHL., in Eur J Haematol, vol. 46, n. 1, Gen 1991, pp. 33-7, PMID 1988304.
- ^ N. Haim, K. Drumea; R. Epelbaum; M. Ben-Shahar, Dexamethasone, cytarabine, ifosfamide, and cisplatin as salvage therapy in non-Hodgkin lymphoma., in Am J Clin Oncol, vol. 22, n. 1, Feb 1999, pp. 47-50, PMID 10025380.
- ^ C. Visco, S. Finotto; R. Zambello; R. Paolini; A. Menin; R. Zanotti; F. Zaja; G. Semenzato; G. Pizzolo; ES. D'Amore; F. Rodeghiero, Combination of rituximab, bendamustine, and cytarabine for patients with mantle-cell non-Hodgkin lymphoma ineligible for intensive regimens or autologous transplantation., in J Clin Oncol, vol. 31, n. 11, Apr 2013, pp. 1442-9, DOI:10.1200/JCO.2012.45.9842, PMID 23401442.
- ^ CM. Davis, JV. VanDersarl; CA. Coltman, Failure of cytarabine in varicella-zoster infections., in JAMA, vol. 224, n. 1, Apr 1973, pp. 122-3, PMID 4347648.
- ^ SC. Schimpff, CL. Fortner; WH. Greene; PH. Wiernik, Cytosine arabinoside for localized herpes zoster in patients with cancer: failure in a controlled trial., in J Infect Dis, vol. 130, n. 6, Dic 1974, pp. 673-6, PMID 4372276.
- ^ RF. Betts, DA. Zaky; RG. Douglas; G. Royer, Ineffectiveness of subcutaneous cytosine arabinoside in localized herpes zoster., in Ann Intern Med, vol. 82, n. 6, Giu 1975, pp. 778-83, PMID 166586.
- ^ DA. Stevens, GW. Jordan; TF. Waddell; TC. Merigan, Adverse effect of cytosine arabinoside on disseminated zoster in a controlled trial., in N Engl J Med, vol. 289, n. 17, Ott 1973, pp. 873-8, DOI:10.1056/NEJM197310252891701, PMID 4354007.
- ^ CB. Lauter, EJ. Bailey; AM. Lerner, Assessment of cytosine arabinoside as an antiviral agent in humans., in Antimicrob Agents Chemother, vol. 6, n. 5, Nov 1974, pp. 598-602, PMID 15825312.
- ^ S. Reykdal, R. Sham; P. Kouides, Cytarabine-induced pericarditis: a case report and review of the literature of the cardio-pulmonary complications of cytarabine therapy., in Leuk Res, vol. 19, n. 2, Feb 1995, pp. 141-4, PMID 7869742.
- ^ CI. Truica, SR. Frankel, Acute rhabdomyolysis as a complication of cytarabine chemotherapy for acute myeloid leukemia: case report and review of literature., in Am J Hematol, vol. 70, n. 4, Ago 2002, pp. 320-3, DOI:10.1002/ajh.10152, PMID 12210815.
- ^ D. Malapert, JD. Degos, [Painful legs and moving toes. Neuropathy caused by cytarabine]., in Rev Neurol (Paris), vol. 145, n. 12, 1989, pp. 869-71, PMID 2559449.
- ^ BJ. Bolwell, PA. Cassileth; RP. Gale, High dose cytarabine: a review., in Leukemia, vol. 2, n. 5, Mag 1988, pp. 253-60, PMID 3287015.
- ^ H. Hasle, Cerebellar toxicity during cytarabine therapy associated with renal insufficiency., in Cancer Chemother Pharmacol, vol. 27, n. 1, 1990, pp. 76-8, PMID 2245495.
- ^ WJ. Baker, GL. Royer; RB. Weiss, Cytarabine and neurologic toxicity., in J Clin Oncol, vol. 9, n. 4, Apr 1991, pp. 679-93, PMID 1648599.
- ^ N. Cole, BE. Gibson, High-dose cytosine arabinoside in the treatment of acute myeloid leukaemia., in Blood Rev, vol. 11, n. 1, Mar 1997, pp. 39-45, PMID 9218105.
- ^ SS. Shah, ME. Rybak; TW. Griffin, The cytarabine syndrome in an adult., in Cancer Treat Rep, vol. 67, n. 4, Apr 1983, pp. 405-6, PMID 6601987.
- ^ A. Manoharan, The cytarabine syndrome in adults., in Aust N Z J Med, vol. 15, n. 4, Ago 1985, pp. 451-2, PMID 3866543.
- ^ WJ. Chng, Cytarabine syndrome revisited., in Br J Haematol, vol. 122, n. 6, Set 2003, p. 875, PMID 12956755.
- ^ T. Ek, J. Abrahamsson, The paediatric cytarabine syndrome can be viewed as a drug-induced cytokine release syndrome., in Br J Haematol, vol. 124, n. 5, Mar 2004, p. 691, PMID 14871258.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su citarabina
Collegamenti esterni
modifica- (EN) cytarabine, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.