Elettrocardiogramma
L'elettrocardiogramma (denotato con la sigla ECG o EKG[N 1]) è una tecnica medica consistente nella riproduzione grafica dell'attività elettrica del cuore registrata sulla superficie del corpo, in particolare del corpo umano.
| Elettrocardiogramma | |
|---|---|
Procedura medica 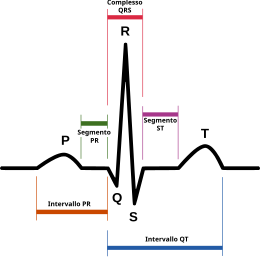 Schema di un elettrocardiogramma: onda P, intervallo PR, complesso QRS, segmento ST, onda T, onda U, intervallo QT  Ritmo sinusale normale | |
| Tipo | Cardiologica |
| Classificazione e risorse esterne | |
| ICD-10 | R94.31 |
| ICD-9 | 89.52 |
| MeSH | D004562 |
| MedlinePlus | 003868 |
| Sinonimi | |
| ECG, EKG | |
Sulla superficie del corpo umano (come in tutti gli animali dotati di muscolo cardiaco), in particolare a livello del tronco, sono presenti campi elettrici di bassa intensità che sono principalmente dovuti alle periodiche depolarizzazioni e ripolarizzazioni del cuore.[3] I potenziali elettrici prodotti dal muscolo cardiaco sono la somma di minime differenze di potenziale generate dalle singole cellule muscolari cardiache.[4] Queste piccole tensioni sono registrabili attraverso un apparecchio denominato elettrocardiografo, modificato e migliorato da Willem Einthoven e Étienne-Jules Marey nel 1903 per derivazione diretta da un galvanometro a corda.[4] Molte delle regole fissate da Einthoven sussistono in epoca moderna e costituiscono la base per interpretare molti aspetti dell'attuale ECG.[4]
Grazie alla conversione dell'energia elettrica in energia meccanica,[3] le variazioni elettriche producono il movimento di un "meccanismo o sistema scrivente".[5] L'energia elettrica è adeguatamente amplificata in modo da poter trascrivere escursioni abbastanza ampie che consentano la registrazione di un segnale leggibile. Le deflessioni vengono impresse su carta, che si muove a velocità costante a contatto con il sistema che riporta sulla carta le onde registrate in funzione del tempo.[6] Contemporaneamente all'oscillazione verticale delle linee prodotte dalle variazioni di potenziale, la carta scorre verso sinistra.[5] Questa sincronizzazione permette di riportare il movimento verticale su un piano orizzontale, registrando le oscillazioni in rapporto alla loro durata nel tempo.[3]
Nell'ECG a 12 derivazioni, quattro elettrodi sono posizionati sugli arti del paziente e sei sulla superficie del torace. Quindi il potenziale elettrico complessivo del cuore viene misurato in dodici punti ("derivazioni") e viene registrato per un determinato periodo di tempo, in genere dieci secondi.[7] In questo modo, l'ampiezza e la direzione generali della depolarizzazione elettrica del cuore vengono catturate in ogni momento e per tutto il ciclo cardiaco.[8]
L'elettrocardiogramma è usato per numerosissimi scopi clinici.[3] Tra i più frequenti vi sono: misurare la frequenza e il ritmo dei battiti cardiaci, verificare le dimensioni e la posizione delle camere cardiache (ad esempio nella destrocardia), individuare la presenza di possibili danni al miocardio o al sistema di conduzione, controllare gli effetti indotti dai farmaci e verificare la buona funzionalità di un pacemaker.[9]
1) ECG con indicazione dell'origine cardiaca del QRS;
2) cellule cardiache depolarizzate;
3) onde positive o negative in base all'attraversamento della corrente nel dipolo;
4) rappresentazione schematica delle derivazioni;
5) mappatura delle regioni del cuore sull'ECG.
Storia
modificaNel XIX secolo divenne chiaro che il cuore umano generava elettricità. Nel 1836 il fisico italiano Carlo Matteucci iniziò i suoi studi di elettrofisiologia all'università di Pisa.[10] Nel 1842 pubblicò i risultati delle sue sperimentazioni con la "pila muscolare", (una colonna di segmenti di muscolo), della rana.[11][12][13] Nel 1844 Matteucci nel suo trattato di elettrofisiologia descrisse l'attività elettrica della muscolatura cardiaca, attività dimostrata utilizzando una "pila muscolare" di cuore di piccione.[14] Nel 1878 J.S. Burdon Sanderson e F.J.M. Page, due fisiologi britannici, collegarono gli elettrodi di un galvanometro alla base e all'apice del cuore di rana e descrissero per la prima volta la variazione del potenziale elettrico associata al ciclo cardiaco.[15]
Dalle osservazioni sperimentali si passò ben presto agli studi clinici.[16] Alexander Muirhead, un ingegnere elettronico, è noto per aver collegato dei fili al polso di un paziente febbrile per ottenere una registrazione del battito cardiaco nel 1872 al St Bartholomew's Hospital.[17] Il primo sistematico approccio al cuore dal punto di vista elettrico fu fatto da Augustus Desiré Waller, al St Mary's Hospital a Paddington, Londra. Nel 1887 Waller pubblicò il primo elettrocardiogramma, ottenuto usando un elettrometro capillare di Lippmann con elettrodi posti sul torace e sul dorso, dimostrando anche che l'attività elettrica del cuore precede la contrazione.[18] Nel 1911 si poterono apprezzare le prime applicazioni cliniche derivate dal suo lavoro.[18] Il suo elettrocardiografo consisteva in un elettrometro capillare fissato a un proiettore. La traccia del battito cardiaco fu proiettata su una lastra fotografica che a sua volta fu fissata a un trenino giocattolo: ciò permise di registrare un battito cardiaco in tempo reale.
Il passo in avanti decisivo fu compiuto da Willem Einthoven con il suo galvanometro, costruito nel 1903.[19] Questo apparecchio era molto più preciso dell'analogo strumento usato da Waller.[20] Einthoven introdusse il termine elettrocardiogramma nel 1893.[13] Assegnò le lettere dell'alfabeto «P, Q, R, S, T» alle varie onde, partendo arbitrariamente dalla lettera P che era stata già usata da Cartesio per indicare i punti successivi di una curva nei suoi studi sulla rifrazione: questo potrebbe essere uno dei motivi che portarono lo studioso alla scelta delle lettere.[21] Snellen, il biografo ufficiale di Einthoven, scrisse a tal riguardo:
«The primary reason for changing the letters from ABCD to PQRST was to eliminate confusion [...]. I believe that Einthoven recognized, perhaps as an afterthought, that by choosing PQRST he allowed space to add letters before P and after T.»
«La ragione principale per cambiare le lettere da ABCD a PQRST era quella di eliminare la confusione [...]. Credo che Einthoven avesse riconosciuto, forse come ripensamento, che scegliendo PQRST avrebbe lasciato spazio per aggiungere lettere prima di P e dopo T.»
Questo apparecchio permise la descrizione di vari tracciati elettrocardiografici, associati a diverse malattie cardiovascolari.[22] Per questa scoperta nel 1924 Willem Einthoven fu insignito del Premio Nobel per la medicina.[23] A quell'epoca l'elettrocardiografo era un voluminoso apparecchio di laboratorio, ancora ignoto ai clinici.
Nel 1937 Tarō Takemi inventò la prima macchina elettrocardiografica portatile.[24]
L'importanza per la diagnosi medica andò di pari passo con la scrittura di testi sempre più ricchi di informazioni: il primo trattato italiano di elettrocardiografia, che gettò le basi dell'interpretazione clinica dell'ECG, fu pubblicato nel 1948 da Daniele Sibilia, cui si deve l'introduzione di questa disciplina in Italia[25].
Sebbene i principi di base di quell'epoca siano tuttora in uso, molti progressi sono stati fatti nell'elettrocardiografia nel corso degli anni. Nel tempo la strumentazione si è notevolmente evoluta e sono disponibili sistemi elettronici compatti che spesso includono l'interpretazione computerizzata dell'elettrocardiogramma.[26]
Alcune applicazioni della metodica permettono a livello ambulatoriale di utilizzare la registrazione Holter nei pazienti che presentano sintomi fugaci ma indicativi per possibili aritmie e richiedono un monitoraggio di almeno 24 ore degli eventi elettrici cardiaci.
Tracciato dell'elettrocardiogramma
modifica1) Potenziale del nodo senoatriale; 2) Potenziale del miocardio atriale; 3) Potenziale del nodo atrioventricolare; 4) Potenziale del fascio di His; 5) Potenziale di una branca del fascio di His; 6) Potenziale delle fibre del Purkinje; 7) Potenziale del miocardio ventricolare.
Il principio su cui si basa la misurazione dell'attività elettrica del cuore è prettamente fisiologico: l'insorgere degli impulsi nel miocardio porta alla generazione di differenze di potenziale che variano nello spazio e nel tempo e che possono essere acquisite tramite degli elettrodi. L'acquisizione della differenza di potenziale da parte di elettrodi posti sulla superficie corporea avviene grazie alla conducibilità del liquido interstiziale del corpo umano. Il segnale acquisito viene trasformato nel tracciato elettrocardiografico che rappresenta il metodo più facile, meno dispendioso e più pratico per osservare se l'attività elettrica del cuore è normale oppure se sono presenti patologie di natura meccanica o bioelettrica. Il normale tracciato ECG presenta un aspetto caratteristico: il tracciato è caratterizzato da una sequenza di deflessioni positive e negative, denominate «onde», separate da alcuni tratti rettilinei, denominati «segmenti». La sequenza che si ripete a ogni ciclo cardiaco.[27].
Per convenzione, il tracciato ECG è riportato su carta millimetrata con il tempo in ascissa (un secondo ogni 25 mm) e l'ampiezza in ordinata (un millivolt ogni 10 mm).
La carta elettrocardiografica ha una quadrettatura di dimensioni standard: le linee orizzontali e verticali sono esattamente a 1 mm di distanza; come riferimento visivo, ogni 5 linee orizzontali e verticali, se ne riporta una più marcata. L'asse orizzontale, leggendo da sinistra a destra, rappresenta il «tempo». Alla velocità standard della carta di 25 mm/s, ogni mm rappresenta 0,04 secondi. L'asse verticale corrisponde all'«ampiezza» delle varie componenti elettrocardiografiche.[28]
Durante ogni battito si susseguono, in una progressione ordinata, onde di depolarizzazione che incominciano dalle cellule pacemaker nel nodo senoatriale, si diffondono attraverso gli atri, passano attraverso il nodo atrioventricolare e proseguono nel fascio di His e nelle fibre del Purkinje,che si estendono verso il basso e a sinistra abbracciando entrambi i ventricoli. Questo modello ordinato di depolarizzazione dà origine al caratteristico tracciato dell'elettrocardiogramma. Le deflessioni registrate sulla superficie corporea rappresentano la somma delle depolarizzazioni o delle ripolarizzazioni di tutte le cellule miocardiche che, in ogni particolare momento, vengono attivate simultaneamente, poiché il miocardio è un sincizio funzionale.
Dato che le cellule cardiache non sottostanno a una depolarizzazione e ripolarizzazione simultanea, l'aspetto dell'ECG ha una forma particolare, completamente diversa dalle registrazioni di una singola cellula o di un piccolo gruppo di cellule.[3] L'aspetto delle onde è determinato dallo stato elettrico presente negli elettrodi posizionati nelle diverse parti del corpo. Uno spostamento verso l'alto è detto «positivo», uno verso il basso «negativo».[5] L'estensione verticale, o «ampiezza», dello spostamento rappresenta l'intensità del potenziale elettrico presente, momento per momento, nel sincizio miocardico: quindi l'ampiezza verticale sarà tanto maggiore quanto più grande è il potenziale elettrico registrato e in particolare normalmente maggiore nelle deflessioni di origine ventricolare rispetto a quelle atriali. Invece le misurazioni orizzontali forniscono l'istante in cui l'evento si verifica.[29] L'intero tracciato va letto da sinistra a destra.[3]
L'ECG è composto da onde positive («P, R, T») e negative («Q, S»). La positività o negatività è riferita alla «linea isoelettrica» che rappresenta lo zero ed è la linea di base dell'elettrocardiogramma. L'isoelettrica è fondamentale per l'interpretazione, specie del segmento ST, che viene considerato nella norma solo se non si discosta da essa di oltre 1 mm, sia in alto sia in basso.[5]
Le onde dell'elettrocardiogramma
modificaSecondo le convenzioni adottate a livello internazionale, tramite il segnale ECG è possibile osservare le onde PQRST, corrispondenti alle fasi del ciclo cardiaco. L'ECG di soggetti sani è costituito da onde PQRST normali, dalla forma tipica. Al contrario, l’ECG di soggetti con condizioni cardiache patologiche o anomale presenta onde PQRST che deviano dalla norma in termini di forma e tempo. La forma del segnale ECG, e in particolare dell’intervallo QT, dipende dalla variabilità della frequenza cardiaca [30].
Onda P
modificaL'onda P è la prima onda che si identifica nel ciclo. È un'immagine derivante dalla depolarizzazione degli atri in risposta all’attivazione del nodo seno-atriale[31][32]. È indice del tempo necessario all’impulso elettrico affinché si diffonda ad entrambi gli atri; questo indice di latenza è utile per identificare malattie cardiache. Dato che la sistole atriale, cioè la contrazione degli atri, non è molto forte, l'onda P è di piccole dimensioni, con ampiezza uguale o inferiore a 0,4 mV, la sua durata varia da 60 ms a 120 ms[30] e la sua forma è associata a condizioni di ipertrofia atriale e della conduzione atrioventricolare. Tipicamente l'onda P non è caratterizzata da altri picchi. Infine, l'assenza di un'onda P può implicare un blocco seno atriale[33].
Tratto PQ
modificaIl tratto PQ è piatto e senza alcuna onda; fa riferimento al tempo che intercorre dall’attivazione degli atri all’attivazione dei ventricoli. La sua normale lunghezza è compresa tra 12 ms e 20 ms[30].
Intervallo PR
modificaL'intervallo PR va dall'inizio dell'onda P all’inizio del complesso QRS. In condizioni cardiache normali, l'ampiezza di quest’onda è di 0,12-0,20 s [31].
Complesso QRS
modificaIl complesso QRS è un segnale che deriva dalla depolarizzazione dei ventricoli e costituito dal susseguirsi delle onde Q, R e S. L’onda Q è breve e decrescente e coincide con la depolarizzazione del setto, l’onda R (picchi R) è un picco positivo molto alto, è lunga e stretta e rappresenta la depolarizzazione dell'apice del ventricolo sinistro, l’onda S è piccola, discendente ed equivale alla depolarizzazione delle regioni basali e posteriori del ventricolo sinistro. Quando il cuore è in una condizione normale, la durata del complesso QRS varia da 60 ms a 90 ms. Ogni alterazione del complesso QRS indica la probabile presenza di anomalie o malattie cardiache, quali ad esempio aritmia, fibrillazione ed infarto [30][31].
Segmento ST
modificaIl segmento ST va dalla fine del complesso QRS all'inizio dell'onda T. Questo tratto, equivalente alla baseline del segnale ECG, corrisponde all'intervallo di tempo in cui i ventricoli si contraggono e tornano a riposo [30][31]. La sua normale durata varia da 230 ms a 460 ms. Un’alterazione di questo segmento può suggerire problemi ischemici [30].
Onda T
modificaL'onda T è l’onda derivante dalla ripolarizzazione dei ventricoli, ovvero il momento in cui i ventricoli hanno terminato la loro fase di attivazione e sono pronti per una nuova contrazione [30][31]. Non sempre è identificabile in quanto può essere di ampiezza molto piccola. La sua durata varia tra 100 ms e 250 ms ed ogni alterazione potrebbe indicare ipertrofia cardiaca, insufficienza cardiaca e cardiopatia ischemica [30]. Quest’ultima, i cui sintomi cardiaci sono soffio cardiaco e dolore toracico, sono indicati da onde T negative [33].
Intervallo QT
modificaL'intervallo QT rappresenta la sistole elettrica, ovvero il periodo di tempo in cui avviene la depolarizzazione e ripolarizzazione dei ventricoli. La lunghezza di questo intervallo varia tra 350 ms e 440 ms [30].
Onda U
modificaL'onda U segue l'onda T e proviene anch’essa dalla ripolarizzazione ventricolare. Non è sempre apprezzabile in un elettrocardiogramma perché spesso di dimensioni minime. La sua durata è compresa tra 185 ms e 228 ms [30].
Determinazione della frequenza cardiaca
modificaUna frequenza cardiaca regolare può essere facilmente stimata misurando l'intervallo fra due complessi QRS.[34]
Il tracciato ECG è rappresentato su carta millimetrata che scorre alla velocità di 25 mm al secondo (cinque quadrati con lato di 5 mm rappresentano 1 secondo): la frequenza cardiaca è l'inverso del tempo trascorso tra due picchi "R" successivi.[35]
Esempio: un complesso QRS ogni quattro quadrati da 5 millimetri significa che la frequenza è circa 75 bpm (battiti al minuto). Infatti, dato che ogni quadrato da 5 mm corrisponde a 0,2 s, quattro quadrati corrispondono a 0,8; si calcola la frequenza dividendo 60 s (1 minuto) per 0,8 s, ovvero 75 bpm.
Più semplicemente: dato che ci sono 300 quadrati in un minuto, la frequenza di un complesso QRS che si verifichi ogni due quadrati è 150 bpm, pari a 300 diviso 2. Analogamente, i complessi che si verificano ogni quattro quadrati hanno una frequenza di 300 diviso 4, cioè 75/min.[34] Un complesso QRS ogni sei quadrati ha una frequenza di 300 diviso 6, cioè 50 bpm e così via.[34]
In caso di ritmo irregolare, per esempio durante una fibrillazione atriale, ogni metodo di calcolo basato sulla distanza fra due battiti è inapplicabile[36], pertanto si considerano i battiti in un determinato arco di tempo. Generalmente si opta per due periodi di tre secondi ciascuno, in cui si contano i QRS e li si moltiplica per 10, in modo da esprimere la frequenza in battiti al minuto.[36]
Sono riconosciuti diversi metodi per la misurazione della frequenza, ma quasi sempre ci si riferisce all'utilizzo di un «regolo»: a un battito se si considera la distanza fra due "R"[37] e a tre battiti, se vengono considerate tre "R", cosa che permette una misura più accurata per effetto della media.[35][37]
Il dipolo elettrico e il dipolo cardiaco
modificaIl cuore dal punto di vista elettrico è, in prima approssimazione, modellizzabile come un dipolo. Se si isola una fibra miocardica, ponendo due elettrodi (A e B) all'inizio e alla fine della fibra e collegandoli a un voltmetro, si misura una differenza di potenziale. In condizioni di riposo, il voltmetro non segnerà nulla perché in condizioni di riposo l'intera superficie esterna della cellula è positiva rispetto all'interno (il citoplasma) che è negativo. Essendo la superficie esterna della fibra isopotenziale, non si ha alcun passaggio di corrente nello strumento.
Quando la fibra viene eccitata il potenziale d'azione comincia a diffondersi. Laddove il potenziale d'azione si propaga, la polarità tra esterno e interno della fibra si inverte: l'esterno diviene negativo e l'interno diviene positivo. Ciò accade perché, durante il potenziale d'azione, si verifica il fenomeno dell'inversione di carica da positiva a negativa della superficie cellulare a causa dell'apertura dei canali ionici di membrana. Di conseguenza l'elettrodo che è posto sulla parte interessata dalla depolarizzazione sarà a un potenziale negativo rispetto all'altro. Nel caso di una miocellula è l'elettrodo A che viene investito per primo dal potenziale d'azione: esso sarà quindi negativo, al contrario dell'elettrodo B che, essendo posto su una parte di fibra a riposo, rimane ancora positivo. Si parla in questo caso di dipolo in movimento.
Ogni singola fibra cardiaca durante il potenziale d'azione si comporta come un dipolo, pertanto l'attività elettrica di ogni singola fibra miocardica può essere rappresentata da un vettore elettrico o vettore di dipolo. L'elettrocardiogramma non registra l'attività elettrica per singola fibra, ma quella del miocardio nel suo insieme. Tuttavia la massa cardiaca si comporta anche a livello elettrico come un sincizio, per cui l'intero miocardio può essere considerato come un unico dipolo, caratterizzato da un proprio vettore: il vettore cardiaco. Infatti in ogni istante vengono contemporaneamente attivate numerose fibre, ognuna delle quali produce il suo potenziale elettrico, il suo vettore di dipolo. La somma di questi vettori istantanei costituisce il vettore cardiaco, il vettore risultante dell'attività elettrica del cuore in toto.
La registrazione dell'attività elettrica cardiaca
modificaI dipoli in movimento delle fibre miocardiche, prodotti dai potenziali d’azione, generano nell'organismo un campo elettrico che può essere registrato sulla superficie corporea. Ponendo due elettrodi in punti diversi di questo campo elettrico è, infatti, possibile registrare la differenza di potenziale che si viene a creare nel campo stesso in seguito al propagarsi ordinato (dagli atri verso i ventricoli) del dipolo cardiaco.
A livello di registrazione dell'ECG, se ne desume che: l'elettrodo che vede il fronte d'onda avvicinarsi diventa positivo rispetto a quello che lo vede allontanarsi. Nel caso invece in cui si pongano due elettrodi A e A' perpendicolari al propagarsi dell'impulso, la misurazione del voltmetro sarà nulla, perché il fronte d'onda investe i due elettrodi contemporaneamente e non vi sarà differenza di potenziale.
Se l'elettrocardiogramma costituisce la rappresentazione grafica delle differenze di potenziale registrate nel campo elettrico cardiaco, la rappresentazione visiva del vettore cardiaco costituisce invece il vettorcardiogramma. Per poter arrivare alla costruzione di un vettorcardiogramma è stato usato un artificio matematico, ricorrendo a una grandezza vettoriale, il vettore dipolo, al posto di una grandezza scalare (la differenza di potenziale), come nel caso dell'elettrocardiogramma. Sulla congiungente degli elettrodi, che viene chiamata «derivazione», viene rilevata la proiezione del vettore dipolo. Di conseguenza due elettrodi paralleli al vettore misurano la differenza di potenziale massima, due elettrodi perpendicolari non misurano nulla. Combinando le proiezioni sulle diverse derivate è possibile avere una rappresentazione bidimensionale o tridimensionale del vettore dipolo, che costituisce appunto il vettorcardiogramma.
È necessario introdurre più di una derivazione per mappare il cuore in tutta la sua superficie e tali derivazioni debbono avere posizioni diverse. In definitiva, in ogni derivazione si registrano gli stessi eventi, presi da diversi punti di vista elettrici, esattamente come un soggetto fotografico può essere ripreso da diverse angolazioni: il soggetto non cambia, ma la prospettiva è diversa in ogni foto.[39][40] Poiché non siamo in grado di visualizzare direttamente l'attività cardiaca, le diverse derivazioni sono utilizzate per avere una visione totale e completa della sequenza di attivazione del cuore.[39]
Le derivazioni elettrocardiografiche
modificaÈ noto che per registrare un elettrocardiogramma è necessario disporre di elettrodi posti sulla superficie corporea, formando delle derivazioni sistemate in maniera tale da poter analizzare al meglio le variazioni del vettore dipolo del cuore. Per poter registrare i potenziali, si poggiano sul corpo 10 elettrodi: 4 periferici (polsi e caviglie) e 6 precordiali, così da registrare 12 derivazioni.[39][40] Nella registrazione bipolare si utilizza una coppia di elettrodi esploranti, mentre in quella unipolare si impiega un solo elettrodo esplorante e si registra la differenza di potenziale tra esso e un elettrodo indifferente a potenziale zero. Le derivazioni sono così nominate:
- derivazioni bipolari degli arti: DI, DII, DIII;[40]
- derivazioni unipolari degli arti: aVR, aVL, aVF;[40]
- derivazioni precordiali: V1, V2, V3, V4, V5, V6.[40]
Derivazioni bipolari
modificaNelle derivazioni bipolari si usano due coppie di elettrodi posizionati rispettivamente la prima sul polso destro e polso sinistro, la seconda su caviglia destra e caviglia sinistra. Si definisce linea di derivazione la congiungente il punto di applicazione virtuale degli elettrodi; in questo modo viene a formarsi, con questa disposizione degli elettrodi, un triangolo equilatero, noto come il triangolo di Einthoven, che ha al suo centro il cuore.[41][42]
Per queste derivazioni è necessario porre delle convenzioni tali per cui:
- in DI il tracciato va verso l'alto quando la spalla sinistra è positiva rispetto alla destra;
- in DII il tracciato va verso l'alto quando la gamba sinistra è positiva rispetto alla spalla destra;
- in DIII il tracciato va verso l'alto quando la gamba sinistra è positiva rispetto alla spalla sinistra.
Si consideri che a questo punto si hanno 3 derivazioni e che il piano frontale su cui noi dobbiamo analizzare il vettore dipolo è di 360°: ne deriva che si ha una suddivisione del piano in tre parti da 120° ciascuna. Questo tuttavia non è sufficiente per registrare in maniera adeguata tutti gli eventuali cambiamenti del vettore, pertanto si rese necessario individuare altre derivazioni che permettessero una migliore valutazione degli eventi: ecco il motivo per il quale si misero a punto le derivazioni "aumentate" di Goldberger.
Derivazioni unipolari aumentate di Goldberger
modificaLe derivazioni aVR, aVL, aVF esplorano il piano frontale lungo le bisettrici degli angoli del triangolo di Einthoven, derivano dagli stessi tre elettrodi di DI - DII - DIII, ma usano il terminale centrale di Goldberger come polo negativo.
Insieme con le derivazioni DI, DII, DIII, le derivazioni degli arti aumentate «aVR, aVL e aVF» costituiscono la base del sistema di riferimento esassiale, che viene utilizzato per calcolare l'asse elettrico del cuore nel piano frontale.
Il terminale centrale di Goldberger è una combinazione di input provenienti dai due elettrodi degli arti, con un'associazione diversa per ciascuna derivazione aumentata. Fu definito come "il polo negativo": collegando gli estremi di ciascuna derivazione con due resistenze uguali e utilizzando la giunzione tra di esse come riferimento, rispetto all'elettrodo posto sul vertice opposto del triangolo, si ottenne la registrazione lungo altre tre direttrici, corrispondenti appunto alle bisettrici del triangolo stesso.
In questo modo, considerando la giunzione delle due resistenze come l'elettrodo di riferimento e gli elettrodi su spalla sinistra-destra-gamba sinistra come elettrodi esploranti, si ottengono le tre derivazioni unipolari degli arti. Esse sono denominate:
- Vfoot (VF)-aVF fra punto centrale delle spalle e la gamba sinistra:
- Vright (VR)-aVR tra punto centrale spalla sinistra-gamba e spalla destra:
- Vleft (VL)-aVL tra punto centrale spalla destra-gamba e spalla sinistra:
Anche in questo caso è necessario dare delle convenzioni:
- tutti i valori ottenuti vengono amplificati, in modo da poter essere raffrontati con quelli delle derivazioni bipolari e si indicano con aVR, aVL e aVF;
- per convenzione il "meccanismo scrivente" va verso l'alto quando l'elettrodo esplorante diviene positivo rispetto a quello di riferimento, ovvero quando l'onda di depolarizzazione va verso l'elettrodo esplorante;
- poiché nella derivazione aVR, il tracciato diviene negativo, per facilitare la lettura si moltiplica questo segnale per -1 (questa è un'operazione che l'elettrocardiografo attua automaticamente).
Così facendo, si è potuti arrivare a esplorare l'attività cardiaca con 6 derivazioni che ci permettono di dividere il piano frontale in zone da 30° l'una, dandoci un dettaglio abbastanza accurato, ma non sufficiente, dell'attività cardiaca[41].
Derivazioni unipolari precordiali di Wilson
modificaVi era comunque la necessità di avere una maggior definizione dell'attività cardiaca e per questo furono approntati degli elettrodi che fossero abbastanza vicini al cuore, al contrario di quelli delle derivazioni uni e bipolari che si trovavano lontane. In particolare questi nuovi elettrodi sono utili per identificare e localizzare, in maniera molto più precisa, delle lesioni che potrebbero sfuggire con l'uso delle sole altre derivazioni, e per analizzare il vettore della depolarizzazione cardiaca sul piano trasversale (orizzontale), diverso da quello frontale precedentemente analizzato e disposto perpendicolarmente a esso.
Si usa in questo caso un elettrodo di riferimento, detto di Wilson, ottenuto come media dei potenziali di Einthoven, e sei elettrodi esploranti posti rispettivamente:[40]
- V1: nel 4º spazio intercostale sulla linea parasternale destra;
- V2: nel 4º spazio intercostale sulla linea parasternale sinistra;
- V3: tra V2 e V4;
- V4: nel 5º spazio intercostale sulla linea emiclaveare sinistra, corrispondente alla punta cardiaca;
- V5: nel 5º spazio intercostale sulla linea ascellare anteriore sinistra;
- V6: nel 5º spazio intercostale sulla linea ascellare media sinistra.
I sei elettrodi precordiali fungono da poli positivi per le sei derivazioni precordiali corrispondenti. Il terminale centrale di Wilson è usato come polo negativo.[41]
Con le precordiali di Wilson, si è arrivati ad avere 12 derivazioni che permettono una completa e particolare analisi dell'attività elettrica del cuore in toto.[41] In realtà si possono identificare altre derivazioni, utilizzate molto più raramente, per situazioni specifiche come la destrocardia (derivazioni destre: da V2R a V5R) [43] o l'infarto miocardico posteriore (derivazioni precordiali posteriori: da V7 a V9).[43] . In caso di un arto amputato, l'elettrodo verrà posizionato nella parte del moncone presente.
Asse cardiaco
modificaIl cuore ha diversi assi elettrici (ciascun asse corrisponde alla direzione di un vettore di dipolo), ma il più comune è l'asse del complesso QRS (i riferimenti all'asse cardiaco implicitamente si riferiscono all'asse del QRS, poiché rappresenta la massa ventricolare e quindi la parte maggiore del muscolo cardiaco). Ogni asse può essere determinato con il metodo del parallelogramma per ottenere un numero che rappresenta i gradi di deviazione dall'asse di simmetria del corpo (o asse di riferimento zero). L'asse del QRS rappresenta la direzione del fronte d'onda della depolarizzazione ventricolare (o vettore elettrico medio) nel piano frontale.
È spesso sufficiente classificare l'asse cardiaco in una delle tre varianti: normale, deviato a sinistra (definito anche «deviazione assiale sinistra») o deviato a destra (anche definita «deviazione assiale destra»). I dati sulla popolazione mostrano che il normale asse del QRS è compreso fra -30° e +105° con 0° lungo il DI, positivo in sede inferiore e negativo in superiore (descritto graficamente dal sistema di riferimento esassiale).[44] Oltre +90°/+105° si parla di deviazione assiale destra e oltre -30° di deviazione assiale sinistra (il terzo quadrante compreso tra 90° e 180° è molto raro ed è un asse indeterminato).
Il modo più pratico per usare il sistema esassiale è invertire la polarità della derivazione aVR e presentare i complessi ECG nell'ordine (aVL, DI, -aVR, DII, aVF, DIII); quindi determinare la direzione del QRS: in quella derivazione ci sono le ampiezze positive massime – questa direzione è l'asse elettrico – come si può vedere dallo schema. Esempio: se la derivazione DI ha la massima ampiezza (superiore a aVL o a -aVR), l'asse è di circa 0°. Viceversa, se la derivazione DIII ha l'ampiezza più negativa significa che il vettore si allontana dalla stessa, cioè andrà verso i -60°.
Possiamo utilizzare anche un altro sistema: si individua la derivazione più isoelettrica fra DI, DII, DIII, aVR, aVL e aVF, quindi si individua il raggio corrispondente sul sistema di riferimento esassiale. Il punto che si troverà alla perpendicolare risulterà essere l'asse elettrico del cuore. Esempio: se la derivazione più isoelettrica è aVL, la derivazione perpendicolare sul sistema di riferimento esassiale è il DII. Se DII è positivo sull'ECG, l'asse elettrico sarà di circa +60°.
L'asse del QRS normale è generalmente diretto "in basso e a sinistra", seguendo l'orientamento anatomico del cuore all'interno del torace. La tabella seguente riassume le caratteristiche dell'asse cardiaco.
| Classificazione | Angolo | Note |
|---|---|---|
| Normale | −30° a +90°/105°** | Normale |
| Deviazione assiale sinistra | −30° a -90° | Può indicare ipertrofia ventricolare sinistra, emiblocco anteriore sinistro, o, se presenti delle piccole "onde q" inferiori, un infarto miocardico inferiore pregresso[45][46] |
| Deviazione assiale destra | +90°/105** a +180° | Può indicare ipertrofia ventricolare destra, emiblocco posteriore sinistro, o, se presenti delle piccole "onde q" laterali, un infarto miocardico laterale pregresso[47] |
| Asse indeterminato | -180°/+180° a −90° | Raramente visibile[48] |
**Un asse normale può essere compreso tra +90° o +105° a seconda delle classificazioni usate.
Lo sviluppo in multipolo
modificaStudi sempre più accurati a partire dagli anni quaranta e cinquanta negli Stati Uniti hanno dimostrato che il comportamento elettrico del cuore è più simile a un multipolo che a un dipolo.
Il lavoro pionieristico dei due ricercatori Nelson e Gabor[49] puntò sul fatto che la teoria del dipolo fosse inadeguata e valesse solo come approssimazione per grandi distanze dalle regioni dove sono situati i dipoli. I loro studi permisero un nuovo approccio all'interpretazione dell'ECG.[50]
Le diverse ricerche cliniche portarono alla ricostruzione del cuore attraverso la sua "mappatura elettrica": una mappa è un insieme di «n» componenti, ciascuna delle quali rappresenta il valore del potenziale cardiaco misurato a un certo istante di tempo in un punto preciso della superficie del tronco. Pertanto si può considerare una mappa come un'«istantanea» di come si distribuisce il potenziale elettrico sul torace. Per avere una buona rappresentazione delle mappe ECG gli studiosi ricorsero all'interpolazione con un sistema di armoniche sferiche. In pratica il cosiddetto sviluppo in multipolo consiste in uno sviluppo ortogonale del potenziale di superficie in armoniche sferiche, immaginando il torace come una porzione di cilindro con sezione circolare.[51]
Una ricostruzione molto buona delle mappe, tale da preservare un grande numero di dettagli, può essere ottenuta ricorrendo ad almeno 64 armoniche sferiche: questo significherebbe che la mappa del potenziale può essere ricostruita facilmente attraverso 64 segnali ECG da diverse posizioni sul torace. È importante ricordare che la mappatura del cuore viene utilizzata non negli esami di routine, ma solo nei laboratori di emodinamica per procedure di ablazione da utilizzare in determinate aritmie come la fibrillazione atriale o la tachicardia sopraventricolare.[52]
Calcolo biomedico e diagnostica elettrocardiografica
modificaL'elettrocardiogramma a 12 derivazioni (ECG) è la tecnologia più utilizzata nella cardiologia clinica. È fondamentale per la gestione di pazienti con infarto miocardico acuto, sospetta ischemia cardiaca, aritmie cardiache, insufficienza cardiaca e dispositivi cardiaci impiantabili. In contrasto con molte altre tecniche utilizzate in cardiologia, l'ECG è semplice da eseguire, l'apparecchio è piccolo e portatile, facilmente disponibile, e quindi particolarmente utile sotto tutti i punti di vista, anche se considerassimo quelli economici. Nonostante la metodica sia ormai "vetusta", la ricerca non si è mai fermata e anzi nel 2015 una review ne ha sottolineato l'importanza anche associata alla vettorcardiografia a 3 derivazioni. Questo ha facilitato l'utilizzo dell'elettrocardiografia e della vettorcardiografia combinate senza la necessità di un sistema di registrazione differente e speciale.[53]
L'interpretazione standard dell'ECG si basa principalmente sulla valutazione visiva diretta, ma progressi nel calcolo biomedico e nell'elaborazione dei segnali (come per gli studi del multipole expansion), uniti alla potenza computazionale disponibile, hanno permesso la ricerca e l'applicazione di nuove e interessanti opzioni per l'analisi ECG pertinenti a tutti i campi della cardiologia. Numerosi indicatori ECG digitali e tecnologie ECG avanzate hanno prodotto risultati interessanti.[54] In questa ricerca la componente chiave del sistema di mappatura è rappresentato dai 252 elettrodi incorporati in un giubbotto che può essere facilmente posizionato sul torace del paziente. Con il giubbotto indossato, una scansione tomografica computerizzata (CT) ottiene la precisa relazione anatomica tra gli elettrodi sul gilet e la superficie epicardica del cuore. Una volta definita l'anatomia, possono essere calcolati sino a 1.500 elettrocardiogrammi unipolari che verranno poi processati dal sistema digitale.[54] Tale metodica necessita di un ulteriore perfezionamento e una più ampia validazione in grandi coorti di pazienti non selezionate, ma la sua utilità sarà tanto maggiore quanto più sarà introdotta nella pratica clinica, sostituendosi, potenzialmente, a esami molto più invasivi e costosi.[54]
Diagnosi elettrocardiografiche
modificaL'utilità dell'ECG risulta evidente nel monitoraggio e nella diagnosi medica sia per quanto riguarda situazioni normali, sia nella gestione di situazioni patologiche derivanti da cause fisiche, chimiche, fisiologiche o patologiche. L'obiettivo generale è quello di ottenere informazioni sulla struttura e sulla funzione del cuore. Gli usi medici di queste informazioni sono molteplici e utili nella pratica clinica quotidiana.[27] Si riportano solo alcune delle indicazioni che richiedono l'esecuzione di un elettrocardiogramma:
- controllo della frequenza cardiaca,
- valutazione del ritmo cardiaco, se le aritmie sono percepite mediante il polso arterioso o sintomi come le palpitazioni,
- monitoraggio di aritmie cardiache note,
- screening della cardiomiopatia ipertrofica nei soggetti che si accingono a praticare sport a livello agonistico,
- monitoraggio degli effetti di un farmaco sul cuore (ad es. prolungamento del QT indotto da farmaci),
- valutazione della presenza di eventuali slivellamenti del tratto isoelettrico (ad esempio uno slivellamento del tratto ST può essere indice di ischemia miocardica),
- alterazioni delle varie onde elettriche che possono indicare anomalie morfologiche delle camere cardiache.
Ritmi sinusali fisiologici
modifica-
Aritmia sinusale: aumento fasico della frequenza cardiaca in ispirazione (per aumentato ritorno venoso) e rallentamento in espirazione (effetto vagale)
-
Bradicardia sinusale: si ha con l'abbassamento della frequenza cardiaca al di sotto di 60 battiti al minuto
-
Tachicardia sinusale: si ha con l'innalzamento della frequenza cardiaca al di sopra di 100 battiti al minuto
-
Extrasistole ventricolare: è un battito cardiaco prematuro, ossia un evento elettrico del muscolo cardiaco che avviene prima del previsto, alterando la successione regolare dei battiti nel ritmo sinusale.[55]
Alcuni ritmi secondari a disturbi della conduzione elettrica
modifica- Ritmi atriali:
-
Fibrillazione atriale: è una patologia elettrica degli atri, che presenta una caratteristica costante: l'attivazione elettrica rapida e apparentemente caotica del tessuto atriale. Il tracciato superiore mostra le fini onde della fibrillazione (freccia rossa) e assenza dell'onda P, in contrapposizione all'isoelettrica "pulita" del ritmo sinusale nel secondo tracciato, che evidenzia la presenza dell'onda P (freccia blu).[55]
-
Flutter atriale: è un'aritmia sopraventricolare con contrazione degli atri molto rapida e sincronizzata, dove la frequenza atriale può arrivare a 250-350 impulsi al minuto. Un aspetto caratteristico è la presenza di onde con il tipico aspetto a «denti di sega».
-
Tachicardia parossistica sopraventricolare: è un ritmo cardiaco ad alta frequenza, che origina al di sopra del ventricoli. Non sono visibili le onde P e la frequenza è in genere superiore ai 150 batt/min.
- Ritmi ventricolari:
-
Tachicardia ventricolare: è un'aritmia ipercinetica caratterizzata da una frequenza ventricolare maggiore di 100 batt/min.[55] Le onde comuni dell'ECG non sono più riconoscibili, infatti l'origine degli impulsi elettrici è a livello ventricolare e ciò comporta uno slargamento dei complessi QRS, che appaiono regolari, generalmente caratterizzati da una sola morfologia (in tal caso si parla di battiti monomorfi).
-
Flutter ventricolare: caratterizzato da onde ampie e sinusoidali con frequenze che oscillano fra i 150 e i 300 batt/min. Tale aritmia necessita di defibrillazione, poiché determina in tempi rapidi una sincope con collasso emodinamico.[56]
-
Fibrillazione ventricolare è un'aritmia cardiaca rapidissima, caotica, che provoca contrazioni non coordinate del muscolo cardiaco e deve essere riconvertita rapidamente con la defibrillazione. L'aspetto del tracciato è caratterizzato dalla presenza di fini onde, desincronizzate.[55][56]
-
Asistolia: con tale termine si indica l'assenza dell'attività cardiaca, che deve essere sostituita prontamente dal massaggio cardiaco e dal posizionamento di un pacemaker temporaneo.[55]
Alterazioni secondarie a patologie cardiocircolatorie
modifica-
Infarto miocardico acuto anteriore esteso: il segmento ST è sopralivellato nelle derivazioni anteriori DI, DII, V1, V2, V3, V4, V5, V6 e sottolivellato nelle derivazioni speculari inferiori DIII.
-
Infarto miocardico acuto infero-laterale: il segmento ST è sopralivellato nelle derivazioni inferiori DII, DIII, aVF e sottolivellato nelle derivazioni speculari anteriori DI, aVL, V2, V3, V6
-
L'ECG mostra un sopraslivellamento di ST con Tachicardia, Emiblocco anteriore sinistro, Infarto miocardico anteriore (attacco cardiaco). Legenda: ST sopralivellato nelle derivazioni anteriori DI, aVL, V1, V2, V3, V4, V5, ST sottolivellato nelle derivazioni inferiori DII, DIII, aVF
- Ischemia: produce un sottoslivellamento o un sopraslivellamento del segmento ST, a seconda se la lesione sia intramurale, coinvolga cioè solo la porzione interna del miocardio o transmurale che attraversa l'intero spessore del miocardio. L'ischemia talvolta può non essere associata a una modificazione immediata del tratto ST nelle prime ore dalla insorgenza sintomatologica per cui l'elemento diagnostico deve essere sempre interpretato da specialisti e integrato dal dosaggio enzimatico. Il sovra- o sottoslivellamento di ST è spesso associato all'inversione dell'onda T, che rappresenta la "memoria elettrica" della recente ischemia[57].
Note
modifica- Annotazioni
- ^ L'abbreviazione «EKG», derivata dal tedesco Elektrokardiogramm, entrò nell'uso soprattutto negli Stati Uniti dall'inizio del XX secolo [1], quando la medicina tedesca era all'avanguardia nello studio della metodica. Al giorno d'oggi, il manuale di stile dell'American Medical Association (AMA Manual of Style: A Guide for Authors and Editors) che influenza buona parte delle pubblicazioni mediche statunitensi, prescrive la sigla «ECG» invece di «EKG».[2] Le due sigle in uso sono comunque derivate dalle indicazioni del New Latin-International scientific vocabulary, che unì elektro- (affine a electro-) a kardi- (affine a cardi-), derivando quest'ultimo dal greco antico καρδία, -ας?, kardía, -as, "cuore").
- Fonti
- ^ Definizione inglese, EKG. Dizionari online Oxford Archiviato il 15 febbraio 2018 in Internet Archive.
- ^ (EN) AMA Manual of Style: A Guide for Authors and Editors, su amamanualofstyle.com. URL consultato il 21 febbraio 2018 (archiviato il 24 febbraio 2018)
- ^ a b c d e f Phillips-Feeney, pp. 18-20.
- ^ a b c Scheidt, p. 7.
- ^ a b c d IPASVI Enna, L'Elettrocardiogramma (PDF), su ipasvienna.it, pp. 12-16. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 28 aprile 2018).
- ^ IPASVI Enna, L'Elettrocardiogramma (PDF), su ipasvienna.it, pp. 72-83. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 28 aprile 2018).
- ^ Scheidt, pp. 8-9.
- ^ ECG- semplificato. Aswini Kumar M.D., su lifehugger.com, LifeHugger. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 2 ottobre 2017).
- ^ Braunwald, p. 108.
- ^ Turkel, p.150.
- ^ (EN) ECG timeline - History of the electrocardiogram, su ecglibrary.com. URL consultato il 2 febbraio 2018 (archiviato il 6 ottobre 2017).
- ^ (FR) C. Matteucci, Sur un phénomène physiologique produit par les muscles en contraction., in Ann Chim Phys, vol. 6, n. 339-341, 1842.
- ^ a b (EN) M. AlGhatrif, A brief review: history to understand fundamentals of electrocardiography, in J. Community Hosp. Intern. Med. Perspect., vol. 2, n. 1, 2012, DOI:10.3402/jchimp.v2i1.14383. URL consultato il 31 gennaio 2018 (archiviato il 28 aprile 2018).
- ^ (FR) Traité des phénomènes électro-physiologiques des animaux, Parigi, Chez Fortin, Masson et C Libraires, 1844, p. 60.
- ^ (EN) J.S. Burdon Sanderson, Experimental relating to the rhythmical and excitatory motions of the ventricle of the heart of the frog, and of the electrical phenomena which accompany them, in Proc. Royal Soc. London, vol. 27, 1878, pp. 410-414. URL consultato il 31 gennaio 2018 (archiviato dall'url originale l'8 agosto 2016).
- ^ (EN) J. Burnett, The origins of the electrocardiograph as a clinical instrument (PDF), in Med. Hist. Suppl., vol. 5, 1985, pp. 53-76. URL consultato il 31 gennaio 2018 (archiviato il 28 aprile 2018).
- ^ (EN) R. M. Birse et al., Muirhead, Alexander, su oxforddnb.com, Oxford Dictionary of National Biography 2004 - (fonte originale è la biografia scritta dalla moglie - Elizabeth Muirhead, Alexandernn Muirhead, 1848-1920, Oxford, Blackwell: stampata privatamente nel 1926). (archiviato il 9 dicembre 2017).
- ^ a b (EN) A.D. Waller, A Demonstration on Man of Electromotive Changes accompanying the Heart's Beat, in J Physiol, vol. 8, n. 5, 1887, pp. 229-34, PMC 1485094, PMID 16991463 (archiviato il 28 aprile 2018).
- ^ (EN) I. Ershler, Willem Einthoven--the man. The string galvanometer electrocardiograph, in Arch Intern Med, 148(2), febbraio 1988, pp. 453-455, DOI:10.1001/archinte.1988.00380020197025, PMID 3277566.
- ^ (EN) M. Rivera-Ruiz, Einthoven's string galvanometer: the first electrocardiograph, in Tex. Heart Inst. J., vol. 35, 2008, pp. 174-178 (archiviato il 25 settembre 2016).
- ^ (EN) J.W. Hurst, Naming of the Waves in the ECG, With a Brief Account of Their Genesis, in Circulation, vol. 98, n. 18, 3 November 1998, pp. 1937–42, DOI:10.1161/01.CIR.98.18.1937, PMID 9799216 (archiviato il 9 dicembre 2017).
- ^ (EN) M. Rivera-Ruiz et al., Einthoven's String Galvanometer: The First Electrocardiograph, in Texas Heart Institute journal / from the Texas Heart Institute of St. Luke's Episcopal Hospital, Texas Children's Hospital, vol. 35, n. 2, Settembre 1927, pp. 174–8, PMC 2435435, PMID 18612490 (archiviato il 25 settembre 2016).
- ^ (EN) J.K. Cooper, Electrocardiography 100 years ago. Origins, pioneers, and contributors, in N Engl J Med, vol. 315, n. 7, 1986, pp. 461–4, DOI:10.1056/NEJM198608143150721, PMID 3526152.
- ^ (EN) Dr. Taro Takemi, in Takemi Program in International Health, 27 agosto 2012. URL consultato l'8 dicembre 2017 (archiviato il 7 marzo 2016).
- ^ Sibilia
- ^ L. Vella, Enciclopedia medica italiana - Aggiornamento alla seconda edizione, Firenze, USES, 1991, pp. 2438-2444. URL consultato il 18 febbraio 2018 (archiviato il 19 febbraio 2018).
- ^ a b Costantini, 2012.
- ^ IPASVI Enna, L'Elettrocardiogramma (PDF), su ipasvienna.it, pp. 29-32. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 28 aprile 2018).
- ^ IPASVI Enna, L'Elettrocardiogramma (PDF), su ipasvienna.it, pp. 27-28. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 28 aprile 2018).
- ^ a b c d e f g h i j (EN) Mario Merone, Paolo Soda e Mario Sansone, ECG databases for biometric systems: A systematic review, in Expert Systems with Applications, vol. 67, 2017-01, pp. 189–202, DOI:10.1016/j.eswa.2016.09.030. URL consultato il 16 giugno 2022.
- ^ a b c d e (EN) Putri Madona, Rahmat Ilias Basti e Muhammad Mahrus Zain, PQRST wave detection on ECG signals, in Gaceta Sanitaria, vol. 35, 2021, pp. S364–S369, DOI:10.1016/j.gaceta.2021.10.052. URL consultato il 16 giugno 2022.
- ^ Anthony H. Kashou, Hajira Basit e Lovely Chhabra, Physiology, Sinoatrial Node, StatPearls Publishing, 2022. URL consultato il 16 giugno 2022.
- ^ a b (EN) Tae Wuk Bae e Kee Koo Kwon, ECG PQRST complex detector and heart rate variability analysis using temporal characteristics of fiducial points, in Biomedical Signal Processing and Control, vol. 66, 2021-04, pp. 102291, DOI:10.1016/j.bspc.2020.102291. URL consultato il 16 giugno 2022.
- ^ a b c Scheidt, p. 18.
- ^ a b Phillips-Feeney, pp. 35-39.
- ^ a b Scheidt, p. 20.
- ^ a b IPASVI Enna, L'Elettrocardiogramma (PDF), su ipasvienna.it, pp. 31-32. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 28 aprile 2018).
- ^ (EN) H. Yang, S. Bukkapatnam , R. Komanduri, Spatiotemporal representation of cardiac vectorcardiogram (VCG) signals, in BioMedical Engineering OnLine, 2012, DOI:10.1186/1475-925X-11-16, PMC 3439290, PMID 22463593.
- ^ a b c Phillips-Feeney, pp. 39-45.
- ^ a b c d e f IPASVI Enna, L'Elettrocardiogramma (PDF), su ipasvienna.it, pp. 37-42. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 28 aprile 2018).
- ^ a b c d Guyton, 2012.
- ^ (EN) B.E. Jin et al., A simple device to illustrate the Einthoven triangle, in Advances in Physiology Education, vol. 36, n. 4, dicembre 2012, pp. 319–324, DOI:10.1152/advan.00029.2012, ISSN 1043-4046, PMC 3776430, PMID 23209014 (archiviato il 19 maggio 2014).
- ^ a b Derivazioni ecgrafiche (PDF), su medtriennalisl.campusnet.unito.it, p. 5. URL consultato il 28 giugno 2024.
- ^ Surawicz, p.12.
- ^ (EN) P. Saltzman et al., Br Heart J, vol. 28, n. 5, settembre 1966, pp. 703-8, PMID 5911566.
- ^ (EN) E.N. Coleman, Ventricular hypertrophy and the electrical axis of the, in Br Heart J, vol. 24, marzo 1962, pp. 139-43, PMID 13880469.
- ^ (EN) A. Castellanos et al., Significance of complete right bundle-branch block with right axis deviation in absence of right ventricular hypertrophy., in Br Heart J, vol. 32, n. 1, gennaio 1970, pp. 85-92, PMID 5417851.
- ^ (EN) A.L. Goldberger, The genesis of indeterminate axis: a quantitative vectorcardiographic analysis., in J Electrocardiol, vol. 15, n. 3, 1982, pp. 221-6, PMID 7119630.
- ^ (EN) D. Gabor e C.V. Nelson, Determination of the resultant dipole of the heart from measurement on the body surface, in J App Phys, vol. 25, 1954, pp. 423-416.
- ^ (EN) P.C. Voukydis, Application of the Gabor-Nelson theory in electrocardiography, in Medical and biological engineering, vol. 10, n. 2, marzo 1972, pp. 223–229.
- ^ (FR) B. Taccardi, Contribution à la détermination quantitative des erreurs de la vectorcardiographie, in Critical Reviews in Biomedical Engineering, vol. 8, n. 3, 1982, p. 277.
- ^ Ablazione transcatetere con Sistema Carto, su humanitas.it. URL consultato il 19 febbraio 2018 (archiviato il 20 febbraio 2018).
- ^ (EN) S. Man, AC. Maan, MJ. Schalij e CA. Swenne, Vectorcardiographic diagnostic & prognostic information derived from the 12-lead electrocardiogram: Historical review and clinical perspective., in J Electrocardiol, vol. 48, n. 4, pp. 463-75, DOI:10.1016/j.jelectrocard.2015.05.002, PMID 26027545.
- ^ a b c (EN) T. Reichlin et al., Advanced ECG in 2016: is there more than just a tracing? (PDF), in Swiss Med Wkly, vol. 146, 2016, pp. w14303, DOI:10.4414/smw.2016.14303, PMID 27124801 (archiviato dall'url originale il 10 dicembre 2017).
- ^ a b c d e IPASVI Enna, L'Elettrocardiogramma (PDF), su ipasvienna.it, pp. 60-71. URL consultato il 6 dicembre 2017 (archiviato dall'url originale il 28 aprile 2018).
- ^ a b Flutter e fibrillazione ventricolari, su Malattie del cuore di Braunwald X ed.: Trattato di medicina cardiovascolare., books.google.it. URL consultato il 5 gennaio 2018 (archiviato il 6 gennaio 2018).
- ^ L'elettrocardiogramma nella Sindrome coronarica Acuta, su link.springer.com. URL consultato il 19 febbraio 2018.
Bibliografia
modifica- E. Braunwald, Malattie cardiache: un libro di testo di medicina cardiovascolare, 5ª ed., Philadelphia, W.B. Saunders Co., 1997, ISBN 0-7216-5666-8.
- M. Costantini e G. Oreto, Aritmie Cardiache: una diagnosi basata sull'ECG. Casi aritmologici emblematici e dizionario pratico di aritmologia, Ambrosiana / CEA, 2012, ISBN 978-88-08-18267-8.
- M. Costantini, L'elettrocardiogramma - dalle basi fisiologiche alla facile interpretazione, 3ª ed., McGraw-Hill Italia, 2012, ISBN 978-88-386-3649-3.
- (EN) L. Favella et al., La rappresentazione del potenziale elettrocardiografico di superficie a partire da 16 sonde, in Communications and computers. Communications and signal processing in medicine, 1977.
- S. Fiocca et al., Fondamenti di anatomia e fisiologia umana, 2ª ed., Napoli, Sorbona, 2000, pp. 189-277, ISBN 88-7150-024-5.
- (EN) D.B. Geselowitz e O.H. Schmidt, Biological Engineering, McGraw-Hill, 1969, ISBN non esistente.
- A.C. Guyton e J.E. Hall, Fisiologia Medica, 12ª ed., Elsevier, 2012, ISBN 88-214-3427-3.
- R.E. Phillips e M.K. Feeney, I ritmi cardiaci - Guida sistematica all'interpretazione, a cura di E. Papini, 2ª ed., Roma, Verduci Editore, 1983, ISBN 978-88-7620-007-6.
- S. Scheidt, Basi teoriche dell'Elettrocardiografia - ECG, traduzione di M. Carnovali, illustrazioni di Frank H. Netter, 5ª ed., Milano, CIBA-GEIGY Italia, 1992 [1991], ISBN non esistente.
- D. Sibilia, L'Elettrocardiogramma. Tecnica - genesi - significato clinico., Roma, Edizioni dell'Ateneo, 1948, ISBN non esistente.
- (EN) B. Surawicz e T. Knillans, Chou's electrocardiography in clinical practice : adult and pediatric, 6ª ed., Philadelphia, Saunders/Elsevier, 2008, ISBN 1-4160-3774-8.
- (EN) W.J. Turkel, Spark from the Deep, Baltimora, The Johns Hopkins University Press, 2013, ISBN 978-1-4214-0981-8.
Voci correlate
modificaAltri progetti
modifica- Wikizionario contiene il lemma di dizionario «elettrocardiogramma»
- Wikiversità contiene risorse sull'elettrocardiogramma
- Wikimedia Commons contiene immagini o altri file sull'elettrocardiogramma
Collegamenti esterni
modifica- Elettrocardiogramma, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- Elettrocardiogramma, su Vocabolario Treccani, Istituto dell'Enciclopedia Italiana.
- elettrocardiogramma, su sapere.it, De Agostini.