Eptazina
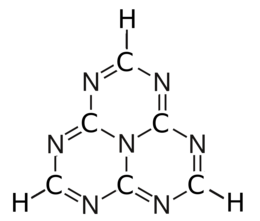
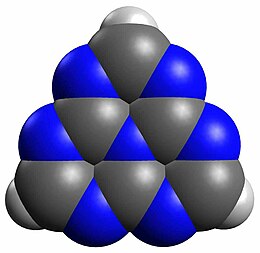
La eptazina o tri-s-triazina è un composto organico con formula C6N7H3, costituito dalla fusione di tre unità s-triazina. In condizioni normali è un solido giallo, debolmente fluorescente, solubile in solventi organici ma decomposto dall'acqua in presenza di luce.[1][2][3]
| Eptazina | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| 1,3,4,6,7,9,9b-Eptaazafenalene | |
| Nomi alternativi | |
| Tri-s-triazina, 1,3,4,6,7,9-Exaazaciclo[3.3.3]azina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H3N7 |
| Massa molecolare (u) | 173,14 |
| Aspetto | solido giallo |
| Numero CAS | |
| PubChem | 136027 |
| SMILES | C1=NC2=NC=NC3=NC=NC(=N1)N23 |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | insolubile |
| Temperatura di fusione | >300 °C (573 K) |
| Indicazioni di sicurezza | |
Il nome eptazina è utilizzato anche per i suoi derivati, dove i tre idrogeni sono stati sostituiti da altri gruppi funzionali. Oligomeri e polimeri dell'eptazina sono stati scoperti già nel 19º secolo, ma il loro studio è stato a lungo ostacolato dalla loro generale insolubilità. Questi composti sono usati come ritardanti di fiamma. I derivati dell'eptazina sono diventati oggetto di interesse per potenziali applicazioni in materiali per ottica non lineare, esplosivi, e per la costruzione di metal organic frameworks.[4][5]
Storia
modificaIn un articolo pubblicato nel 1835 Justus von Liebig riporta che Jöns Jacob Berzelius scoprì che l'accensione del tiocianato mercurico Hg(SCN)2 produceva H2S, acido cianidrico HCN, e un residuo giallo insolubile. Liebig esaminò questo residuo e ne definì la composizione come (C2N3H)n attribuendogli il nome melone.[5][6] Negli anni seguenti Leopold Gmelin e Wilhelm Henneberg prepararono altri composti correlati con quelli preparati da Liebig, chiamandoli melonati e ciamelurati.[7][8][9]
La struttura di questi composti fu chiarita solo nel 1937 da Linus Pauling e James Holmes Sturdivant. Tramite misure di cristallografia a raggi X stabilirono che i composti contenevano un nucleo C6N7 di anelli triazinici fusi, che chiamarono "nucleo ciamelurico".[4][9] La sintesi dell'eptazina vera e propria è stata descritta solo nel 1982.[1]
Struttura molecolare e configurazione elettronica
modificaL'eptazina cristallizza nel sistema ortorombico, gruppo spaziale Pbca, con costanti di reticolo a = 722,5 pm, b = 2719,3 pm, c = 1385,8 pm, 16 unità di formula per cella elementare. La molecola risulta planare.[1]
Secondo Pauling e Sturdivant, il modo migliore di descrivere la configurazione elettronica dell'eptazina è tramite 20 diverse strutture di risonanza, rappresentate nell'immagine successiva. Nelle ultime tre strutture ci sono 6 possibilità distinte dovute a rotazione e inversione speculare della molecola.[9]
Calcoli teorici indicano che nell'eptazina e in alcuni suoi derivati il più basso stato eccitato di tripletto (T1) sia situato ad energia maggiore del più basso singoletto eccitato (S1). È stato quindi sostenuto che l'eptazina costituisca il primo esempio di molecola organica a guscio chiuso che viola la prima regola di Hund.[3]
Note
modificaBibliografia
modifica- (EN) J. Ehrmaier, E. J. Rabe, S. R. Pristash, K. L. Corp e altri, Singlet–Triplet Inversion in Heptazine and in Polymeric Carbon Nitrides, in J. Phys. Chem. A, vol. 123, n. 38, 2019, pp. 8099–8108, DOI:10.1021/acs.jpca.9b06215.
- (DE) L. Gmelin, Ueber einige Verbindungen des Melon's, in Ann. Pharm., vol. 15, n. 3, 1835, pp. 252-258, DOI:10.1002/jlac.18350150306.
- (DE) W. Henneberg, Ueber einige Zersetzungsproducte des Mellonkaliums, in Justus Liebigs Ann. Chem., vol. 73, n. 2, 1850, pp. 228-255, DOI:10.1002/jlac.18500730217.
- (EN) R. S. Hosmane, M. A. Rossman e N. J. Leonard, Synthesis and structure of tri-s-triazine, in J. Am. Chem. Soc., vol. 104, n. 20, 1982, pp. 5497–5499, DOI:10.1021/ja00384a046.
- (DE) J. Liebig, Ueber einige Stickstoffverbindungen, in Ann. Phys., vol. 110, n. 4, 1835, pp. 570-613, DOI:10.1002/andp.18351100403.
- (EN) L. Pauling e J. H. Sturdivant, The Structure of Cyameluric Acid, Hydromelonic Acid and Related Substances, in Proc. Natl. Acad. Sci. U.S.A., vol. 23, n. 12, 1937, pp. 615–620, DOI:10.1073/pnas.23.12.615.
- (EN) A. Schwarzer, T. Saplinova e E. Kroke, Tri-s-triazines (s-heptazines)—From a “mystery molecule” to industrially relevant carbon nitride materials, in Coord. Chem. Rev., vol. 257, n. 13-14, 2013, pp. 2032-2062, DOI:10.1016/j.ccr.2012.12.006.
- (EN) M. Shahbaz, S. Urano, P. R. LeBreton, M. A. Rossman e altri, Tri-s-triazine: synthesis, chemical behavior, and spectroscopic and theoretical probes of valence orbital structure, in J. Am. Chem. Soc., vol. 106, n. 10, 1984, pp. 2805–2811, DOI:10.1021/ja00322a014.
- E. K. Wilson, Old Molecule, New Chemistry. Long-mysterious heptazines are beginning to find use in making carbon nitride materials, su Chemical & Engineering News, 2004. URL consultato il 28 settembre 2022.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su eptazina