Hsp90
Hsp90 è una proteina da shock termico caratterizzata da un peso molecolare di circa 90 kDa (dai cui il nome) presente nelle cellule eucariote, nelle quali svolge un ruolo essenziale per quanto riguarda il ripiegamento e l'attivazione di una determinata clientela di proteine, oltre a esercitare la sua azione di protezione e contrasto dell'effetto denaturante del calore qualora le condizioni ambientali lo richiedano.
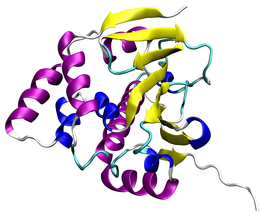
| Heat shock protein 90kDa | |
|---|---|
 | |
| Gene | |
| HUGO | HSP90 |
| Entrez | 3320 |
| Locus | Chr. 14 q32.33 |
| Proteina | |
| OMIM | 140571 |
| UniProt | P07900 |
| PDB | 1BYQ |
Aspetti generali
modificaLe Hsp (heat shock proteins) sono la classe più espressa fra tutte le proteine cellulari, la cui funzione è quella di preservare l'integrità della cellula qualora sia esposta ad elevate temperature.[1] Esse rappresentano circa l'1-2% della quantità di proteine presenti in cellule eucariote in condizioni ambientali normali,[2] fino a raggiungere percentuali del 4-6% nel momento in cui le cellule sono esposte al calore.[3]
Come tutte le proteine da shock termico, essa svolge la funzione di chaperon, ossia assiste il ripiegamento delle proteine in modo da assicurarne una struttura corretta e funzionale, ed inoltre è coinvolta nella trasduzione dei segnali cellulari.
Caratteristiche strutturali
modificaLa struttura di Hsp90 è simile a quella di altre proteine globulari contenenti elementi strutturali secondari comuni (alfa eliche e foglietti beta). Essendo una proteina citoplasmatica essa presenta una regione non polare all'interno e numerosi domini polari all'esterno, così da risultare solubile in acqua. Hsp90 contiene nove alfa-eliche e otto foglietti beta anti-paralleli, che si combinano per formare diversi strati sovrapposti alfa/beta.[4]
Domini
modificaHsp90 presenta quattro domini strutturali:[5][6][7]
- un dominio N-terminale altamente conservato (NTD) di circa 25 kDa
- una regione linker, che collega l'N-terminale con il dominio centrale
- un dominio centrale (MD) di circa 40 kDa
- un dominio C-terminale (CTD) di circa 12 kDa.
Sono state ottenute le strutture cristalline per il dominio N-terminale di Hsp90 di lievito e umano,[8][9][10] per complessi del dominio N-terminale durante l'interazione con inibitori e nucleotidi,[8][9] e per il dominio centrale di Hsp90 di lievito.[11] Hsp90 forma omodimeri nei quali i siti di interazione sono localizzati all'interno del C-terminale nella conformazione aperta del dimero. Nella conformazione chiusa del dimero anche i domini N-terminali risultano in contatto.[12]
Clientela molecolare
modificaIn veste di proteina chaperon, Hsp90 assiste la maturazione di una serie di proteine, fra le quali si annoverano:
- oltre un centinaio di fattori di trascrizione e chinasi
- recettori di steroidi
- proteine p53 mutanti
- la proteina HER2, avente ruolo nel cancro alla mammella.
Non si è ancora trovata una connessione fra le proteine sopracitate, le quali condividono tra loro solamente la necessità della presenza di Hsp90, essenziale per assicurarne una corretta maturazione.
Ruolo nel cancro
modificaSiccome buona parte delle proteine assistite da Hsp90 è coinvolta nella crescita cellulare, ciò la rende un ottimo target per la chemioterapia del cancro. Le cellule cancerose si affidano in maggior misura ad Hsp90 rispetto alle cellule sane, rispondendo quindi in modo più forte ai farmaci che ne inibiscono la funzionalità, rendendo generalmente le terapie basate sulla neutralizzazione di questa proteina relativamente poco tossiche. Ad esempio, tramite lo studio della struttura cristallina di complessi Hsp90-ATP, si è osservato che il sito legante della proteina, caratterizzato da una adenina posizionata in un dominio N-terminale, lega efficacemente anche la geldanamicina, sostanza impiegata in passato come farmaco antitumorale, ma rimossa dal mercato poiché sostituita da farmaci meno tossici.[4] L'inibizione di Hsp90 consegue nella proliferazione di proteine ripiegate in modo errato all'interno delle cellule tumorali, inducendo così il sistema ubiquitina-proteosoma ad eliminare tali proteine, quindi provocando la morte di tali cellule. Hsp90 stabilizza inoltre vari recettori di fattori di crescita[13] e di alcune molecole di segnalazione tra le quali la fosfatidilinositolo-3-chinasi (PI3K) e la proteina chinasica B (AKT), pertanto l'inibizione di Hsp90 può indurre apoptosi attraverso l'inibizione del pathway di segnalazione PI3K/AKT.[8][14] Un altro ruolo importante di Hsp90 nel cancro è la stabilizzazione di proteine mutanti, come v-Src, l'oncogene di fusione Bcr/Abl e forme mutanti di p53 che appaiono durante la trasformazione cellulare. Sembra che Hsp90 possa intervenire per mantenere il corretto ripiegamento delle proteine meno stabili prodotte da mutazioni del DNA, rendendo l'effetto di tali mutazioni fenotipicamente meno rilevante.[15]
Note
modifica- ^ P. Csermely, T. Schnaider, C. Soti, Z. Prohászka, G. Nardai, The 90-kDa molecular chaperone family: structure, function, and clinical applications. A comprehensive review, in Pharmacol. Ther., vol. 79, n. 2, agosto 1998, pp. 129–68, DOI:10.1016/S0163-7258(98)00013-8, PMID 9749880.
- ^ Amere Subbarao Sreedhara, EŁ va Kalmára, Peéter Csermelya, Yu-Fei Shenb, Hsp90 isoforms: functions, expression and clinical importance (PDF), in FEBS Letters, vol. 562, n. 1, 08 03 2004, p. 11.
- ^ G. Crevel, H. Bates, H. Huikeshoven, S. Cotterill, The Drosophila Dpit47 protein is a nuclear Hsp90 co-chaperone that interacts with DNA polymerase alpha [collegamento interrotto], in J. Cell. Sci., vol. 114, n. 11, giugno 2001, pp. 2015–25.
- ^ a b M.P. Goetz, D.O. Toft, M.M. Ames, C. Erlichman, The Hsp90 chaperone complex as a novel target for cancer therapy, in Ann. Oncol., vol. 14, n. 8, agosto 2003, pp. 1169–76, DOI:10.1093/annonc/mdg316, PMID 12881371.
- ^ L.H. Pearl, C. Prodromou, Structure and in vivo function of Hsp90, in Curr. Opin. Struct. Biol., vol. 10, n. 1, febbraio 2000, pp. 46–51, DOI:10.1016/S0959-440X(99)00047-0, PMID 10679459.
- ^ C. Prodromou, L.H. Pearl, Structure and functional relationships of Hsp90, in Curr Cancer Drug Targets, vol. 3, n. 5, ottobre 2003, pp. 301–23, DOI:10.2174/1568009033481877, PMID 14529383.
- ^ L.H. Pearl, C. Prodromou, Structure, function, and mechanism of the Hsp90 molecular chaperone, in Adv. Protein Chem., Advances in Protein Chemistry, vol. 59, 2001, pp. 157–86, DOI:10.1016/S0065-3233(01)59005-1, ISBN 978-0-12-034259-4, PMID 11868271.
- ^ a b c C.E. Stebbins, A.A. Russo, C. Schneider, N. Rosen, F.U. Hartl, N.P. Pavletich, Crystal structure of an Hsp90-geldanamycin complex: targeting of a protein chaperone by an antitumor agent, in Cell, vol. 89, n. 2, aprile 1997, pp. 239–50, DOI:10.1016/S0092-8674(00)80203-2, PMID 9108479.
- ^ a b C. Prodromou, S.M. Roe, R. O'Brien, J.E. Ladbury, P.W. Piper, L.H. Pearl, Identification and structural characterization of the ATP/ADP-binding site in the Hsp90 molecular chaperone, in Cell, vol. 90, n. 1, luglio 1997, pp. 65–75, DOI:10.1016/S0092-8674(00)80314-1, PMID 9230303.
- ^ C. Prodromou, S.M. Roe, P.W. Piper, L.H. Pearl, A molecular clamp in the crystal structure of the N-terminal domain of the yeast Hsp90 chaperone, in Nat. Struct. Biol., vol. 4, n. 6, giugno 1997, pp. 477–82, DOI:10.1038/nsb0697-477, PMID 9187656.
- ^ P. Meyer, C. Prodromou, B. Hu, C. Vaughan, S.M. Roe, B. Panaretou, P.W. Piper, L.H. Pearl, Structural andunctional analysis of the middle segment of hsp90: implications for ATP hydrolysis and client protein and cochaperone interactions, in Mol. Cell, vol. 11, n. 3, marzo 2003, pp. 647–58, DOI:10.1016/S1097-2765(03)00065-0, PMID 12667448.
- ^ P. Meyer, C. Prodromou, B. Hu, C. Vaughan, S.M. Roe, B. Panaretou, P.W. Piper, L.H. Pearl, Structural and functional analysis of the middle segment of hsp90: implications for ATP hydrolysis and client protein and cochaperone interactions, in Mol. Cell, vol. 11, n. 3, marzo 2003, pp. 647–58, DOI:10.1016/S1097-2765(03)00065-0, PMID 12667448.
- ^ A. Sawai, S. Chandarlapaty, H. Greulich, M. Gonen, Q. Ye, C.L. Arteaga, W. Sellers, N. Rosen, D.B. Solit, Inhibition of Hsp90 down-regulates mutant epidermal growth factor receptor (EGFR) expression and sensitizes EGFR mutant tumors to paclitaxel, in Cancer Res., vol. 68, n. 2, gennaio 2008, pp. 589–96, DOI:10.1158/0008-5472.CAN-07-1570, PMID 18199556.
- ^ S.K. Mohsin, H.L. Weiss, M.C. Gutierrez, G.C. Chamness, R. Schiff, M.P. Digiovanna, C.X. Wang, S.G. Hilsenbeck, C.K. Osborne, D.C. Allred, R. Elledge, J.C. Chang, Neoadjuvant trastuzumab induces apoptosis in primary breast cancers, in J. Clin. Oncol., vol. 23, n. 11, aprile 2005, pp. 2460–8, DOI:10.1200/JCO.2005.00.661, PMID 15710948.
- ^ S.K. Calderwood, M.A. Khaleque, D.B. Sawyer, D.R. Ciocca, Heat shock proteins in cancer: chaperones of tumorigenesis, in Trends Biochem. Sci., vol. 31, n. 3, marzo 2006, pp. 164–72, DOI:10.1016/j.tibs.2006.01.006, PMID 16483782.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su Hsp90