Lomitapide
Lomitapide è un farmaco utilizzato per ridurre la colesterolemia nei pazienti adulti con Ipercolesterolemia familiare omozigote, come terapia aggiuntiva alla dieta e ad altri farmaci ipocolesterolemizzanti, con o senza aferesi delle LDL. Lomitapide riduce la sintesi epatica e intestinale delle lipoproteine plasmatiche (VLDL e chilomicroni), agendo come inibitore selettivo della proteina microsomiale di trasporto dei N-trigliceridi (MTP). Il farmaco è commercializzato in Italia con il nome di Lojuxta.
| Lomitapide | |
|---|---|
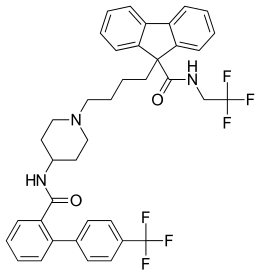 | |
| Nome IUPAC | |
| N-(2,2,2-Trifluoroethyl)-9-[4-[4-[[[4'-(trifluoromethyl)[1,1'-biphenyl]2-yl]carbonyl]amino]-1-piperidinyl]butyl]-9H-fluoren-9-carboxamde | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C39H37F6N3O2 |
| Massa molecolare (u) | 693.719 g/mol |
| Numero CAS | |
| Codice ATC | C10 |
| PubChem | 9853053 |
| DrugBank | DBDB08827 |
| SMILES | C1CN(CCC1NC(=O)C2=CC=CC=C2C3=CC=C(C=C3)C(F)(F)F)CCCCC4(C5=CC=CC=C5C6=CC=CC=C64)C(=O)NCC(F)(F)F |
| Indicazioni di sicurezza | |
Chimica
modificaLomitapide mesilato è un derivato della fluorene-carbossammide, il cui nome chimico (IUPAC) è N-(2,2,2-trifluoroetil)-9-[4-[4-[ [ [4'(trifluorometil)[ 1,1'-bifenil] -2-il] carbonil] amino]-1-piperidinil]butil]-9H-fluorene-9-carbossammide.[1] La molecola è costituita da un nucleo N-eterociclico centrale (piperidina), ai lati opposti del quale si dispongono i due gruppi trifluorurati: fluorene-carbossamidico e bifenil-carbossamidico.
Farmacocinetica
modificaDopo somministrazione orale, l'assorbimento intestinale di Lomitapide si svolge con una cinetica di primo ordine: entro l'intervallo del dosaggio terapeutico (5-60 mg/die), l'assorbimento è proporzionale alla dose somministrata. L'assorbimento è favorito dal pasto, soprattutto se ricco di grassi. La concentrazione plasmatica massima (Cmax) è raggiunta in 6 ore (tmax).[2][3]
Una volta assorbito, il farmaco subisce un importante effetto di "primo passaggio", viene cioè rimosso dal sangue proveniente dall'intestino (circolo portale) ad opera del fegato. Negli studi sugli animali la concentrazione del farmaco nel fegato è risultata circa 200 volte superiore rispetto a quella plasmatica. Ne consegue che la biodisponibilità orale (la percentuale di farmaco che raggiunge la circolazione sistemica) di Lomitapide è soltanto del 7%; il legame alle proteine plasmatiche è >99,8%.[2]
Lomitapide è metabolizzato nel fegato, principalmente ad opera dell'isoenzima 3A4 del citocromo P-450 (CYP3A4): ossidazione, N-dealchilazione ossidativa, glicuronoconiugazione; i metaboliti sono farmacologicamente inattivi.[3][4]
L'eliminazione è sia urinaria (33-35%) che fecale (53-60%).[2][5][4] L’emivita di eliminazione (t1/2) è di circa 39 ore.[3]
Farmacodinamica
modificaA differenza delle tre principali classi di farmaci ipocolesterolemizzanti (statine, ezetimibe e sequestranti degli acidi biliari), Lomitapide agisce indipendentemente dall'espressione dei recettori delle LDL: inibisce la proteina MTP (microsomal triglyceride transfer protein) legandosi ad essa e disattivandola.
La proteina MTP riveste un ruolo essenziale nell’assemblaggio e nella secrezione delle lipoproteine a densità molto bassa (VLDL) e dei chilomicroni, rispettivamente, nelle cellule epatiche (epatociti) e nelle cellule epiteliali intestinali (enterociti). L’MTP è una proteina di trasporto dei lipidi localizzata nel lume del reticolo endoplasmatico.[6] Essa veicola molecole lipidiche (trigliceridi, fosfolipidi e esteri del colesterolo) verso le apoB-lipoproteine nascenti: la proteina apoB viene sintetizzata dai ribosomi in corrispondenza della membrana del reticolo endoplasmatico e, via via che la neosintetizzata proteina si allunga, essa trasloca nel lume del reticolo, dove MTP ne promuove l’associazione con i lipidi (lipidazione).[7][8]
Otre a consentire l’incorporazione dei lipidi nelle lipoproteine nascenti, MTP agisce contemporaneamente come chaperone: interagisce fisicamente con l’apoB e ne guida il corretto ripiegamento tridimensionale, prevenendone la degradazione intracellulare nei proteosomi.[7][9] Gli studi sulla cinetica delle proteine apoB nei soggetti trattati con Lomitapide (1mg/kg) hanno infatti rilevato una riduzione del 70% nella produzione delle apoB.[10] L’importanza della funzione di MTP è indicata dal fatto che una sua mutazione è causa di Apobetalipoproteinemia, una grave malattia del metabolismo lipidico.[11]
Grazie alla inibizione di MTP, dopo 18 mesi di terapia alla dose media 40mg/die, Lomitapide ha abbassato le concentrazioni plasmatiche di colesterolo totale (-35%%) e LDL (-38%) e di trigliceridi (-31%); al contrario la produzione delle apoA-proteine non è risultata significativamente interessata e la concentrazione plasmatica delle HDL è rimasta pressoché invariata.[4][12][13] In accordo con ciò, la concentrazione di farmaco che inibisce del 50% (IC50) la secrezione delle apoB è notevolmente più bassa di quella che inibisce la secrezione delle apoA (0.8 nM vs 6.5 µM).[4]
Quale conseguenza della limitazione della lipidazione delle nuove lipoproteine plasmatiche, la terapia con Lomitapide si accompagna all'accumulo di lipidi negli epatociti e negli enterociti, accumulo che è responsabile, rispettivamente, di steatosi epatica e di malassorbimento dei grassi che vengono così persi nelle feci (steatorrea).[4]
Indicazioni e Controindicazioni
modificaLomitapide è indicato per il trattamento dei pazienti adulti affetti da Ipercolesterolemia familiare omozigote. Tali pazienti presentano un deficit dell'attività dei recettori delle LDL totale (<2% di attività) o parziale (2-25%). La terapia con Lomitapide deve essere associata alla dieta povera di lipidi (<20% delle calorie totali), ad altri farmaci ipocolesterolemizzanti ed eventualmente ad aferesi delle LDL.[2]
Lomitapide è controindicato nelle seguenti condizioni:[2]
Ipersensibilità al principio attivo o agli eccipienti;
Disfunzione epatica moderata o grave (categoria Child-Pugh B o C), persistenza di test di funzionalità epatica anormali o malattie epatiche in fase attiva. Queste controindicazioni sono la conseguenza della tendenza del farmaco ad aumentare il contenuto di lipidi nel fegato (steatosi epatica), con possibilità di evoluzione verso la steatoepatite ed eventuale progressione in cirrosi epatica;
Malattie infiammatorie croniche intestinali, malassorbimento o altra malattia intestinale significativa (Lomitapide causa sovraccarico lipidico degli enterociti);
Concomitante terapia con simvastatina a dosaggio >40mg/die o inibitori forti o moderati di CYP3A4 (vedi interazioni farmacologiche).
Avvertenze e Precauzioni
modificaPer il rischio di effetti negativi sul fegato, è necessario controllare i valori plasmatici degli enzimi epatici (in particolare transaminasi, fosfatasi alcalina, gammaglutammiltransferasi) prima di iniziare la terapia, poi una volta al mese nel primo anno di trattamento, quindi ogni 3 mesi e comunque ad ogni aumento di dosaggio.[2]
In caso di emodialisi non si devono superare i 40 mg/die di Lomitapide.
L'uso di bevande alcoliche non è raccomandato, a ragione del loro effetto epatico (steatosi ed epatotossicità).
Poiché Lomitapide tende a ridurre l’assorbimento intestinale delle sostanze liposolubili, è opportuno integrare la dieta con quantità idonee di vitamina E, acido linoleico e acidi grassi omega-3 (acido eicosapentaenoico e acido docosaesaenoico).[2]
Si deve usare attenzione in caso di pazienti di età pari o superiore ai 65 anni, poiché l'esperienza in questi soggetti è limitata.
Effetti collaterali
modificaIn seguito all'accumulo di lipidi nella mucosa intestinale, nel corso della terapia con Lomitapide compaiono con elevatissima frequenza (>90%) manifestazioni avverse gastrointestinali: diarrea (80%), nausea (65%), dispepsia (38%), vomito (35%); in oltre il 20% dei casi si possono verificare dolore o gonfiore addominale, flatulenza o stipsi.[2] L'adozione di una dieta a basso contenuto lipidico (<20% delle calorie totali) e una graduale definizione del dosaggio di Lomitapide possono migliorare la tollerabilità gastroenterica.
Molto comuni (>10%) sono anche la riduzione dell'appetito e del peso corporeo; comuni (1-10%) astenia e cefalea.
Fra gli eventi avversi obiettivi (segni) i più frequenti (1-10%) comprendono epatomegalia (da steatosi epatica) e manifestazioni cutanee (rash eritematoso, ecchimosi).[2]
Fra le alterazioni dei parametri di laboratorio prevale nettamente (35%) il rialzo delle transaminasi (ALT e AST) oltre 3 volte i valori normali. Tale evento richiede la riduzione del dosaggio del farmaco o la temporanea interruzione della terapia. Sono comuni (1-10%), e legate all'ostacolo all'assorbimento intestinale, le riduzioni delle concentrazioni plasmatiche delle vitamine liposolubili (carotene e vitamine E e K) e del potassio.[2]
Interazioni
modificaInibitori e induttori di CYP3A4
modificaPoiché Lomitapide è metabolizzato nel fegato ad opera soprattutto di CYP3A4, gli inibitori di questo enzima aumentano l'esposizione dell'organismo al farmaco, mentre gli induttori dell'enzima hanno effetto opposto.[2]
Gli inibitori forti e moderati di CYP3A4 (gli antibiotici macrolidi claritromcina ed eritromicina; l'antibiotico chetolide telitromicina; gli antifungini azolici itraconazolo, fluconazolo, miconazolo e ketoconazolo; i calcioantagonisti diltiazem e verapamil; gli antiaritmici dronedarone e amiodarone; l'antidepressivo nefazodone; gli inibitori della proteasi dell’HIV; il succo di pompelmo) sono controindicati in associazione con Lomitapide. Se l'impiego degli inibitori forti o moderati è necessario, allora la somministrazione di Lomitapide deve essere interrotta.[4] Nel caso di inibitori deboli di CYP3A4 (es. atorvastatina, cimetidina, contraccettivi orali a base di estrogeni), l'assunzione di Lomitapide deve avvenire a 12 ore di distanza dall'inibitore debole.
Gli induttori di CYP3A4 (aminoglutetimide, nafcillina, inibitori non nucleosidici della trascrittasi inversa, fenobarbital, rifampicina, carbamazepina, pioglitazone, glucocorticoidi, modafinil e fenitoina) riducono l’effetto di Lomitapide: in caso di co-somministrazione potrebbe essere necessario aumentare la dose di Lomitapide.[2]
Altre interazioni
modificaStatine. Lomitapide aumenta la concentrazione plasmatica delle statine e può aumentare il rischio di miopatia legato a questi farmaci.[2]
Warfarin. Lomitapide aumenta la concentrazione plasmatica di warfarin e ne può aumentare l'effetto anticoagulante.[2]
Farmaci potenzialmente epatotossici. Lomitapide può potenziare l'azione epatotossica di alcuni farmaci (es. amiodarone, tetracicline, paracetamolo ad alti dosaggi).
Substrati della P-glicoproteina (P-pg). Lomitapide inibisce la proteina P-pg che è presente soprattutto negli epiteli della mucosa intestinale, dei dotti biliari e pancreatici, dei tubuli renali, dell'endotelio e della barriera emato-encefalica.[14] P-pg o proteina di resistenza multifarmaco interviene nell'eliminazione di sostanze indesiderate, tra le quali numerosi farmaci. La sua inibizione comporta pertanto un aumento dell'esposizione dell'organismo verso i farmaci substrato della P-pg (es. digossina, immunosoppressori).[2] Qualora fosse necessaria la co-somministrazione di questi farmaci con Lomitapide può essere opportuno ridurne il dosaggio.
Note
modifica- ^ (EN) J.R. Wetterau, An MTP Inhibitor That Normalizes Atherogenic Lipoprotein Levels in WHHL Rabbits, in Science, vol. 282, 1998, pp. 751-754.
- ^ a b c d e f g h i j k l m n o Scheda tecnica (PDF), in EMA. URL consultato il 13 maggio 2018 (archiviato dall'url originale il 12 febbraio 2018).
- ^ a b c (EN) K.A. Davis, Lomitapide: A novel agent for the treatment of homozygous familial hypercholesterolemia (abstract), in Am. J. Health Syst. Pharm., vol. 71, 2014, pp. 1001-1008.
- ^ a b c d e f (EN) M.D. Panno, Lomitapide: a novel drug for homozygous familial hypercholesterolemia. (PDF), in Clin. Lipidol., vol. 9, 2014, pp. 19-32.
- ^ (EN) C.R. Sirtori, Microsomal transfer protein (MTP) inhibition-a novel approach to the treatment of homozygous hypercholesterolemia (abstract), in Ann. Med., vol. 46, 2014, pp. 464-474.
- ^ (EN) A,J, Hooper, Contemporary aspects of the biology and therapeutic regulation of the microsomal triglyceride transfer protein., in Circ. Res., vol. 116, 2015, pp. 193-205.
- ^ a b (EN) A. Bakillah, Decreased secretion of ApoB follows inhibition of ApoB-MTP binding by a novel antagonist (abstract), in Biochem., vol. 39, 2000, pp. 4892-4899.
- ^ (EN) M.M. Hussain, Multiple functions of microsomal triglyceride transfer protein, in Nutr. Metab., vol. 9, 2012, p. 14.
- ^ (EN) M.M. Hussain, Microsomal triglyceride transfer protein and its role in apoB-lipoprotein assembly, in J. Lipid Res., vol. 44, 2003, pp. 22-32.
- ^ (EN) M. Cuchel, Inhibition of microsomal triglyceride transfer protein in familial hypercholesterolemia, in N. Engl. J. Med., vol. 356, 2007, pp. 148-156.
- ^ (EN) F.K. Welty, Hypobetalipoproteinemia and abetalipoproteinemia, in Curr. Opin. Lipidol, vol. 25, 2014, pp. 161–168.
- ^ (EN) A. Vuorio, Inhibition of hepatic microsomal triglyceride transfer protein - a novel therapeutic option for treatment of homozygous familial hypercholesterolemia., in Vasc. Health Risk Manag., vol. 10, 2014, pp. 263-270.
- ^ (EN) M. Cuchel, Efficacy and Safety of a Microsomal Triglyceride Transfer Protein Inhibitor in Homozygous Familial Hypercholesterolemia, in Lancet, vol. 381, 2013, pp. 40–46.
- ^ (EN) A. Lutful, P-glycoprotein Inhibition for Optimal Drug Delivery, in Drug Target Insights, vol. 7, 2013, pp. 27–34.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su lomitapide