Esano
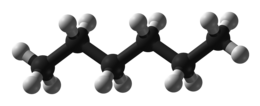
Con il termine esano ci si riferisce ad un qualunque alcano avente formula bruta C6H14 o ad una qualunque miscela di più composti corrispondenti a tale formula (isomeri strutturali) o per antonomasia all'isomero lineare, chiamato più propriamente n-esano[2].
| Esano | |
|---|---|
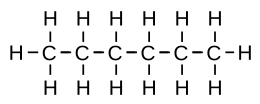 | |
 | |
| Nomi alternativi | |
| n-esano | |
| Caratteristiche generali | |
| Formula bruta o molecolare | CH3(CH2)4CH3 |
| Massa molecolare (u) | 86,18 g/mol |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 203-777-6 |
| PubChem | 8058 |
| SMILES | CCCCCC |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,66 (20 °C) |
| Solubilità in acqua | 0,0095 g/l (20 °C) |
| Temperatura di fusione | −94 °C (179 K) |
| Temperatura di ebollizione | 69 °C (342 K) (1013 hPa) |
| ΔebH0 (kJ·mol−1) | 34,46 KJ/mol |
| Tensione di vapore (Pa) a {{{tensione_di_vapore_temperatura}}} K | 16,94 KPa a 298K |
| Indicazioni di sicurezza | |
| Punto di fiamma | −22 °C (251 K) (vaso chiuso) |
| Limiti di esplosione | 1,0 - 8.1 vol% |
| Temperatura di autoignizione | 240 °C (513 K) |
| Simboli di rischio chimico | |
   
| |
| pericolo | |
| Frasi H | 225 - 304 - 361f - 373 - 315 - 336 - 411 |
| Consigli P | 210 - 240 - 273 - 301+310 - 331 - 302+352 - 403+235 [1] |
A temperatura e pressione ambiente si presenta come un liquido incolore dall'odore di benzina, di cui è un costituente importante, e quasi immiscibile con l'acqua. È un composto estremamente infiammabile, irritante, nocivo, pericoloso per l'ambiente e tossico per il sistema riproduttivo.
È un solvente molto importante, unico a causa della sua bassissima costante dielettrica. È utilizzato nelle reazioni che coinvolgono basi molto forti, ad esempio la preparazione di un reattivo di Grignard poiché non è possibile deprotonare l'esano, in fase condensata, e quindi non interviene nella reazione.
Il suo utilizzo principale è quello di carburante; in miscela con i suoi 5 isomeri costituzionali e con quelli di eptano e ottano forma la comune benzina per autotrazione. È un solvente apolare aprotico, utilizzato per l'estrazione di olio dalle farine delle oleaginose. I residui di lavorazione sono quasi privi di grasso. Durante la tostatura (a 105 °C) il solvente viene quasi completamente recuperato.
Isomeri dell'esano
modificaGli isomeri costituzionali dell'esano sono 5:
| Nome comune | Nome IUPAC | Formula condensata | formule di struttura semplificata |
|---|---|---|---|
| normal-esano n-esano |
esano | CH3(CH2)4CH3 | |
| isoesano | 2-metilpentano | (CH3)2CH(CH2)2CH3 | |
| 3-metilpentano | CH3CH2CH(CH3)CH2CH3 | ||
| 2,3-dimetilbutano | (CH3)2CHCH(CH3)2 | ||
| neoesano | 2,2-dimetilbutano | (CH3)3CCH2CH3 |
Talvolta con il termine esano si indica uno qualsiasi di tali isomeri o una miscela di composizione variabile costituita da questi isomeri.
Tossicità
modificaL'esano-2,5-dione è un metabolita neurotossico dell'esano.[3]
Note
modifica- ^ scheda del n-esano su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ leggi: normal-esano
- ^ Walter J. Krasavage, John L. O'Donoghue, George D. DiVincenzo, Clarence J. Terhaar, The relative neurotoxicity of methyl-n-butyl ketone, n-hexane and their metabolites, in Toxicology and Applied Pharmacology, vol. 52, n. 3, 1980, pp. 433–441, DOI:10.1016/0041-008X(80)90338-5. URL consultato il 24 febbraio 2016.
Altri progetti
modifica- Wikizionario contiene il lemma di dizionario «esano»
- Wikimedia Commons contiene immagini o altri file su esano
Collegamenti esterni
modifica- (EN) hexane, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.