Recettore muscarinico
Il recettore muscarinico è un recettore transmembrana accoppiato a proteine G coinvolto nella trasmissione del segnale all'interno del sistema nervoso parasimpatico.[1] Il loro ligando endogeno è costituito dall'acetilcolina e il loro agonista esogeno muscarina, un alcaloide contenuto nell'Amanita muscaria e in alcune altre specie di funghi velenosi (in particolare specie appartenenti ai generi Inocybe e Clitocybe).[2] La molecola di acetilcolina attiva i recettori muscarinici, permettendo una reazione parasimpatica in tutti gli organi e tessuti in cui il recettore è espresso. I recettori nicotinici sono recettori ionotropici legati a ligando che rispondono anche all'acetilcolina, ma sono principalmente presenti nel sistema nervoso centrale.[2] I recettori muscarinici sono coinvolti nella peristalsi, nella minzione, nella broncocostrizione e in diverse altre reazioni parasimpatiche.[3][4][5] I recettori muscarinici sono un tipo di recettore accoppiato alle proteine G legate a ligando, che funzionano sia come proteine G regolatorie simulative (Gs) che come proteine G regolatorie inibitorie (Gi). La stimolazione dell'acetilcolina attiva la proteina Gq per attivare la PLC e il Ca2+. Esistono cinque diversi sottotipi di recettori che, quando disfunzionali o sovra-stimolati, possono essere bersaglio di vari farmaci agonisti ed antagonisti.[6][7]
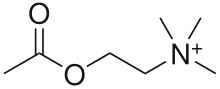
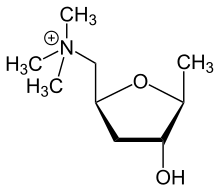
L'unica eccezione a questi recettori sono le ghiandole sudoripare, che possiedono recettori colinergici muscarinici ma fanno parte del sistema nervoso simpatico.
Sottotipi recettoriali
modificaI recettori muscarinici colinergici fanno parte di una vasta famiglia di recettori accoppiati alle proteine G. La loro diversità funzionale deriva dall'interazione con l'acetilcolina e comprende diverse risposte cellulari, tra cui l'inibizione dell'adenilato ciclasi, la degenerazione del fosfoinositide e la regolazione dei canali del potassio. Questi recettori hanno un'influenza significativa sugli effetti dell'acetilcolina sia nel sistema nervoso centrale che in quello periferico.[8][9]
Sottotipo M1 (CHRM1)
modificaIl recettore muscarinico colinergico di tipo 1 svolge un ruolo nella regolazione della broncocostrizione indotta dal nervo vago e nella secrezione acida del tratto gastrointestinale. È espresso maggiormente su prostata, encefalo, ghiandole salivari ed in concentrazione inferiore su ghiandole surrenali, polmoni, derma e stomaco.[10] Il gene responsabile della codifica di questo recettore è localizzato sulla regione 11q13 del cromosoma 11.[8][9]
Sottotipo M2 (CHRM2)
modificaIl recettore muscarinico colinergico di tipo 2 svolge un ruolo importante nella regolazione della bradicardia e nella diminuzione della contrattilità cardiaca. È espresso maggiormente su miocardio, cistifellea e vescica ed in concentrazione inferiore su appendice, encefalo, duodeno, colon, endometrio, placenta, intestino tenue.[10] Per questo gene sono state descritte molteplici varianti di trascritti alternativi. Il gene responsabile della sua codifica è localizzato sulla regione 7q33 del cromosoma 7.[11][12]
Sottotipo M3 (CHRM3)
modificaIl recettore colinergico muscarinico di tipo 3 controlla la contrazione della muscolatura liscia e la sua stimolazione provoca la secrezione di tessuto ghiandolare. È espresso maggiormente su encefalo, ghiandole salivari, esofago ed in concentrazione inferiore su stomaco, pancreas, colon, duodeno, intestino tenue ovaio, vescica, endometrio, fegato, polmoni, tiroide, tesicoli, reni, appendice, surrene e placenta.[10] L'uso di promotori alternativi e lo splicing alternativo producono molteplici varianti di trascritti che presentano specificità tissutali diverse. Il gene responsabile della sua codifica è localizzato sulla regione 1q43 del cromosoma 1.[13][14]
Sottotipo M4 (CHRM4)
modificaLe implicazioni cliniche di questo recettore sono sconosciute; tuttavia, studi su topi collegano la sua funzione all'inibizione dell'adenilato ciclasi. È espresso maggiormente su encefalo, intestino, tessuto linfoide e testicoli.[15] Il gene responsabile della sua codifica è localizzato sulla regione 11p11.2 del cromosoma 11.[16][17]
Sottotipo M5 (CHRM5)
modificaLe implicazioni cliniche di questo recettore sono sconosciute; tuttavia, è noto che la stimolazione di questo recettore aumenta i livelli di AMP ciclico. È espresso maggiormente su placenta, testicoli, encefalo ed in concentrazione inferiore su appendice, surrene, colon, cistifellea, intestino tenue, derma, milza, tessuto linfoide, polmoni, reni e fegato.[10] Il gene responsabile della sua codifica è localizzato sulla regione 15q14 del cromosoma 15.[18][19]
| Sottotipo | Gene | Funzione | PTX (tossina della pertosse) | CTX (tossina colerica) | Effetto | Agonisti[20] | Antagonisti[20] |
|---|---|---|---|---|---|---|---|
| M1 | CHRM1 |
|
no
(si) |
no
(si) |
Gq
(Gi) (Gs): Rallentamento del potenziale eccitatorio postgangliare ↓ K+ conduzione[23][27] |
| |
| M2 | CHRM2 |
|
si | no | Gi | ||
| M3 | CHRM3 |
|
no | no | Gq |
|
|
| M4 | CHRM4 |
|
si | ? | Gi |
| |
| M5 | CHRM5 | no | ? | Gq |
Localizzazione dei recettori
modificaI recettori muscarinici sono ampiamente distribuiti in tutto l'organismo umano e mediano funzioni fisiologiche distinte in base alla loro localizzazione e sottotipo recettoriale.[35] Cinque sottotipi distinti di recettori muscarinici (M1-M5) sono noti esistere, sebbene la localizzazione esatta e il ruolo funzionale di tutti questi sottotipi non siano ancora stati completamente elucidati. In particolare, questi recettori possono svolgere ruoli differenziati ma vitali all'interno dello stesso sistema corporeo, con possibili interazioni tra i sottotipi. Pertanto, una completa comprensione di questi diversi sottotipi di recettori muscarinici risulta essere di grande importanza.
Vescica
modificaIn condizioni normali, la contrattilità del muscolo detrusore umano è principalmente controllata dal sistema nervoso parasimpatico, dove l'acetilcolina (ACh) agisce come principale segnale stimolante sui recettori muscarinici.
Diversi studi indicano che il muscolo detrusore di varie specie, compreso quello umano, contiene tutti i sottotipi dei recettori muscarinici, ma i recettori M2 e M3 risultano predominanti. In particolare, il sottotipo M2 è più numeroso rispetto al sottotipo M3, con un rapporto di 3:1.[36][37] Tuttavia, è il sottotipo M3, sebbene rappresenti una minoranza, che svolge un ruolo fondamentale nella contrazione del muscolo detrusore umano in vitro.[38][39] Questo è dimostrato anche dalla forte correlazione tra l'affinità funzionale nei campioni di detrusore umano isolato e l'affinità dei recettori ricombinanti per una serie di antagonisti muscarinici, che risulta essere maggiore per il sottotipo M3. Ulteriori evidenze che supportano il ruolo funzionale del sottotipo M3 derivano da studi condotti su topi in cui il gene del recettore M3 è stato disattivato (knockout). In strisce di tessuto vescicale prelevate da questi topi, il 95% della contrazione indotta dalla carbacol, una molecola agonista, è mediata dai recettori M3. Questo è evidenziato dal fatto che la risposta contrattile massimale è ridotta al solo 5% rispetto a quella osservata nei topi di tipo selvatico.[40] Tuttavia, i topi knockout per il recettore M3 presentano ancora un pattern di contrazione quasi normale a livello cistometrico, grazie all'attivazione rimanente dei meccanismi purinergici.[41]
Il ruolo funzionale dei recettori M2 nel muscolo detrusore, che costituiscono una popolazione numerosa, rimane ancora oggetto di studio. Un'indagine condotta utilizzando topi knockout per i recettori M2, M3 e M2/M3 ha evidenziato che il recettore M2 potrebbe avere un ruolo nell'indurre le contrazioni vescicali in modo indiretto, potenziando la risposta contrattile all'attivazione dei recettori M3, e potrebbero verificarsi anche contrazioni minori mediata dai recettori M2.[42] In un altro studio condotto su roditori, gli autori suggeriscono che la stimolazione dei recettori M2 potrebbe contribuire all'inibizione del rilassamento mediato dal sistema simpatico (ad esempio, tramite i recettori beta-adrenergici), favorendo così un più efficiente svuotamento della vescica.[43] Un ruolo funzionale per i recettori M2 nella funzione vescicale potrebbe emergere in determinate condizioni patologiche, come osservato negli studi sull'ostruzione del flusso in ratti[44][45] e nelle vesciche neurogene umane.[46] Ad esempio, nella vescica di ratto denervata si osserva un aumento della densità dei recettori M2 (con un corrispondente aumento del rapporto M2:M3), con l'affinità funzionale degli antagonisti muscarinici che si avvicina maggiormente all'affinità per i recettori M2 piuttosto che per i recettori M3.[44] Tuttavia, l'affinità funzionale dell'antagonista selettivo per il recettore M3, 4-DAMP, non differisce tra una vescica di ratto normale e una ostruita.[47] La modulazione simpatica della vescica umana tramite i recettori M2 può essere dedotta anche in base all'innervazione noradrenergica, sebbene scarsa, che è stata dimostrata nel corpo vescicale umano e che aumenta nella regione di deflusso.[48]
Sono stati presentati due studi durante il congresso dell'Associazione Urologica Americana nel 2004, i quali hanno riportato che il recettore M3 svolge un ruolo nella mediazione della risposta contrattile diretta nel tessuto muscolare detrusore umano. Questa osservazione è stata fatta sia nei pazienti affetti da iperattività detrusoriale neurogenica e idiopatica (DO), che nei pazienti con una funzione vescicale normale.[49] Non sono state osservate differenze significative nel contributo dei sottotipi dei recettori nel tessuto patologico durante le contrazioni del detrusore. Gli esperimenti con il carbacolo hanno indicato che la funzione mediata dai recettori muscarinici era potenziata nei tessuti con DO neurogenica e idiopatica rispetto ai tessuti vescicali normali in vitro. L'uso dell'antagonista selettivo del recettore M3, 4-DAMP, ha ridotto la risposta contrattile al carbacolo sia nella vescica normale che in quella con DO neurogenica e idiopatica. L'antagonista selettivo del recettore M2, metoctramina, è stato meno efficace in tutti i tessuti. Tuttavia, non sono state osservate differenze significative nei risultati ottenuti con i due antagonisti.[50] Questo suggerisce che i recettori M2 potrebbero svolgere un ruolo indiretto nella mediazione delle risposte contrattili.
Ricerche in vitro su tessuti vescicali umani e di cavia hanno portato alla teoria che un sistema di cellule interstiziali, simile alle cellule interstiziali di Cajal presenti nell'intestino (miofibroblasti), potrebbe amplificare e coordinare l'attività autonoma del detrusore.[51][52][53] Inoltre, evidenze immunocitochimiche provenienti da roditori hanno dimostrato la presenza di recettori M3 sulle cellule interstiziali nello strato suburoteliale.[54] Si è ipotizzato che queste cellule, che esprimono recettori M3, possano contribuire alla generazione di contrazioni periodiche e che possano essere attivate dall'acetilcolina prodotta e rilasciata dall'urotelio/suburotelio.[55] Secondo questa ipotesi, queste cellule potrebbero attivare l'attività periodica, mentre i neuroni che rilasciano ATP e peptidi all'interno della rete di cellule interstiziali modulerebbero le sensazioni vescicali. È stato dimostrato, ad esempio, che l'attivazione dei recettori colinergici nelle cellule epiteliali dei felini facilita il rilascio di ATP[56], che a sua volta potrebbe attivare i nervi afferenti o i miofibroblasti adiacenti. Pertanto, l'attività periodica inappropriata potrebbe contribuire alla DO e potrebbe essere responsabile della sensazione di "urgenza".
I recettori muscarinici sono anche localizzati pregiunzionalmente sui terminali nervosi colinergici all'interno della vescica, dove i recettori M1 facilitano il rilascio di neurotrasmettitori e i recettori M2/M4 ne inibiscono il rilascio.[57][58] Tuttavia, il ruolo funzionale di questi recettori pregiunzionali rimane ancora poco chiaro.[57][59] Studi in vitro suggeriscono che il recettore M1 sia un importante modulatore del rilascio di acetilcolina e che durante un aumento del traffico nervoso possa favorire una minzione più efficiente. Inoltre, ci sono evidenze che suggeriscono che i recettori pregiunzionali facilitatori possano subire delle modificazioni dopo una lesione del midollo spinale.[60] I recettori M3 ad alta affinità pregiunzionali sui terminali nervosi colinergici vengono sovraespressi nelle vesciche di ratti con lesione cronica del midollo spinale, prendendo il posto dei recettori muscarinici M1 a bassa affinità.[61] Al contrario, si ipotizza che i recettori pregiunzionali inibitori M2 e M4 possano favorire la conservazione dell'urina, con un'attività potenziata in situazioni di traffico nervoso a bassa frequenza, ad esempio in condizioni patologiche come la denervazione vescicale o lesioni del midollo spinale.[62]
È evidente che il controllo della funzione vescicale normale e patologica e il ruolo funzionale dei recettori muscarinici sono estremamente complessi. Non si sa ancora se l'efficacia degli agenti antimuscarinici nel trattamento della OAB sia specifica per un effetto sui recettori M3 presenti nel muscolo detrusore o se anche altri siti recettoriali, come i nervi sensoriali o l'urotelio/suburotelio, contribuiscano all'effetto terapeutico.
Ghiandole salivari
modificaIl sistema parasimpatico svolge un ruolo cruciale nella produzione di saliva attraverso l'attivazione delle cellule sierose e mucose delle strutture acinari delle ghiandole salivari[63], nonché delle cellule sierose presenti nelle ghiandole parotidi. Diversi studi su esseri umani e roditori hanno evidenziato la presenza dei recettori M1 e M3 nelle ghiandole salivari, con una predominanza dei recettori M3 nelle ghiandole parotidi.[64][65][66] Inoltre, studi funzionali su topi e ratti hanno dimostrato che la secrezione della ghiandola sottomandibolare è mediata dai recettori M1 e M3, mentre la secrezione della ghiandola parotide avviene principalmente tramite i recettori M3 (e, eventualmente, M4).[67][68][69] L'attendibilità di tali risultati è confermata dalla loro riproducibilità in diverse modalità di stimolazione della salivazione, sia mediante stimolazione elettrica del sistema parasimpatico che attraverso l'utilizzo di oxotremorina o pilocarpina. Pertanto, i recettori M3 sono fondamentali per il controllo sia delle secrezioni ad alta e bassa viscosità che del volume di saliva, mentre i recettori M1 svolgono un ruolo preponderante nella lubrificazione ad alta viscosità. Queste osservazioni sono state supportate da studi preclinici su ratti e gatti, i quali hanno dimostrato che l'uso di farmaci antagonisti selettivi dei recettori M3 inibisce parzialmente, ma non completamente, le risposte salivari indotte da carbacolo o stimolazione elettrica.[70][71]
Nonostante la salivazione sia principalmente mediata dai recettori M3, l'importanza funzionale di diversi sottotipi di recettori muscarinici nella quantità e qualità della secrezione salivare è evidenziata dal fatto che la salivazione indotta dagli agonisti (utilizzando oxotremorina, pilocarpina o isoproterenolo) è ridotta nel topo privo del recettore M3, ma la cavità buccale rimane lubrificata.[68][72] Al contrario, i topi privi dei recettori M1 e M4 mostrano una risposta intermedia, mentre i topi privi dei recettori M2 e M5 presentano una salivazione normale.[68] Poiché la salivazione indotta dalla pilocarpina è annullata nei topi con doppia delezione dei recettori M1/M3[69] e la secrezione salivare massima indotta dal carbacholo richiede sia i recettori M1 che M3[73], è evidente che la salivazione è mediata da due diversi recettori muscarinici postgiunzionali. Oltre ai recettori postgiunzionali, sono presenti recettori M2 e M1 neuroni che innervano le ghiandole salivari. Questi recettori neuronali hanno un ruolo contributivo nella salivazione inibendo (M2) o potenziando (M1) il rilascio di acetilcolina dai nervi.[74] Nel contesto clinico, alcuni studi hanno mostrato che gli antagonisti selettivi e non selettivi dei recettori muscarinici M3 (con attività su entrambi i recettori M1 e M3) sembrano ridurre la salivazione in proporzioni simili nei pazienti.[75][76][77] Al contrario, in uno studio crossover su 65 pazienti con OAB che confrontava darifenacin con ossibutinina, il trattamento con ossibutinina a rilascio immediato (IR) 5 mg tre volte/die è stato associato a una significativa riduzione (P<0.05) del flusso salivare rispetto a darifenacin a rilascio controllato (CR) (15 mg/die o 30 mg/die).[78] È possibile che, rispetto all'antagonismo di entrambi i sottotipi di recettori, il risparmio dei recettori M1 nelle ghiandole salivari possa contribuire a mantenere una lubrificazione sufficiente per alleviare la sensazione e la gravità della bocca secca. Ciò è supportato da basse percentuali di interruzione del trattamento per bocca secca (<3%) durante il trattamento con darifenacin, basato su un'analisi combinata di tre studi su darifenacin.[79]
Apparato gastrointestinale
modificaAnche se è stato dimostrato che il muscolo liscio dell'intestino contiene tutti e cinque i sottotipi di recettori muscarinici in proporzioni diverse nei cavie[80], si ritiene che i recettori M2 e M3 siano i più importanti dal punto di vista funzionale nell'uomo. Similmente alla vescica, i recettori M2 superano di gran lunga la popolazione dei recettori M3 in una proporzione fino a 4:1 nell'uomo,[81][82] ma i dati provenienti da studi condotti su roditori e cani suggeriscono che il recettore M3 sembra svolgere un ruolo predominante nella stimolazione colinergica della motilità gastrointestinale.[83][84][85][86] Pertanto, l'antagonismo di questi recettori potrebbe contribuire a una riduzione del transito colico. Un ruolo funzionale per gli altri sottotipi di recettori muscarinici, in particolare il recettore M2, sta iniziando a emergere.[72][87] Infatti, la ricerca in vitro utilizzando il muscolo liscio murino ha indicato che i recettori M2 possono avere un contributo maggiore alla contrattilità del tratto gastrointestinale rispetto alla vescica.[72]
Numerosi altri meccanismi di segnalazione, mediati da una varietà di neurotrasmettitori nel sistema nervoso enterico, sembrano svolgere un ruolo importante nel controllo fisiologico della funzione gastrointestinale. I recettori serotoninergici (5-HT) sono stati dimostrati essere importanti nel controllo della motilità e della sensibilità gastrointestinale. Ad esempio, il sottotipo di recettore 5-HT4 media effetti eccitatori[88] e influenza direttamente la secrezione gastrointestinale. Altri meccanismi di segnalazione implicati nel controllo della funzione gastrointestinale includono la Sostanza P e la neurochinina (NK) A che agiscono sui recettori NK1 e NK2, e l'inibizione del rilascio di ossido nitrico. L'interazione complessa tra questi meccanismi aiuta a spiegare perché i topi privi di recettori M3 non presentano problemi gastrointestinali evidenti.[72]
Analogamente alla vescica, molte lacune di conoscenza persistono riguardo al ruolo funzionale dei recettori muscarinici e al contributo di sottotipi specifici all'interno del tratto gastrointestinale. Questi includono il ruolo dei recettori muscarinici espressi dalle cellule interstiziali di Cajal e dai neuroni enterici, il ruolo dei recettori M4 e M5 sul muscolo liscio e i meccanismi di compensazione a lungo termine per la privazione muscarinica. Nel contesto clinico, la stipsi dopo terapia con antagonisti muscarinici viene spesso riportata come uno degli eventi avversi muscarinici classici. In un'analisi combinata di studi clinici con dose fissa con l'antagonista selettivo del recettore M3 darifenacin, è stato osservato un aumento nell'incidenza segnalata di stipsi rispetto al placebo (incidenza per tutte le cause del 14,8% e del 21,3% per darifenacin CR 7,5 e 15 mg/die, rispettivamente, rispetto al 6,2% per il placebo).[79] Sebbene l'incidenza di stipsi sembri essere più alta con darifenacin rispetto ad altri antimuscarinici, un confronto clinico tra darifenacin e l'antagonista non selettivo del recettore muscarinico tolterodina IR ha mostrato che i due agenti erano associati a incidenze simili di uso di lassativi per stipsi e di interruzioni per stipsi.[89] Tuttavia, ulteriori studi dettagliati sono necessari per indagare gli effetti clinici comparativi degli antagonisti selettivi del recettore M3 e non selettivi del recettore muscarinico sul tratto gastrointestinale.
Encefalo
modificaI recettori muscarinici nel cervello attivano una molteplicità di vie di segnalazione importanti per la modulazione dell'eccitabilità neuronale, la plasticità sinaptica e la regolazione di feedback del rilascio di acetilcolina. Tutti e cinque i sottotipi di recettori muscarinici sono espressi nel cervello.[90] Ad esempio, i recettori M1 sono più abbondanti nel neocorteccia, nell'ippocampo e nel neostriato, mentre i recettori M2 si trovano in tutto il cervello. Al contrario, i livelli di recettori M3 sono bassi, mentre i recettori M4 sono abbondanti nel neostriato, e i recettori M5 sono stati localizzati nei neuroni di proiezione della substantia nigra, pars compacta, dell'area tegmentale ventrale e dell'ippocampo.
Localizzazione dei recettori muscarinici all'interno dell'encefalo:[91]
M1: Abbondante nella neocorteccia, nell'ippocampo e nel striato
- Cellule piramidali
- Una piccola frazione sembra essere presente su assoni e terminali
M2: Presente in tutto l'encefalo
- Autorecettore (inibitorio) nell'ippocampo e nella corteccia
- Terminali non-colinergici nell'ippocampo, nella corteccia e nel bulbo olfattorio
- Prosencefalo basale (ad esempio, neuroni gabaergici nel corteccia visiva)
- Talamo
M3: Livelli bassi in tutto l'encefalo
- Ippocampo
- Talamo
- Neuroni gabaergici striatali
M4: Abbondante nello striato; presente anche nella corteccia e nell'ippocampo
- Autorecettore (inibitorio) nello striato
- Neuroni striatali medio-spinosi
- Ippocampo
M5: Neuroni di proiezione della substantia nigra, pars compacta e dell'area ventrale tegmentale; presente anche nell'ippocampo
- Terminali dopaminergici stimolatori nell'accumbens e nello striato GABA, acido gamma-amminobutirrico
I recettori muscarinici presenti nel sistema nervoso centrale (SNC) partecipano attivamente ai processi cognitivi superiori, inclusi l'apprendimento e la memoria. La comunità scientifica concorda generalmente sul fatto che i recettori M1 rivestano un ruolo funzionale rilevante in questo ambito. Ad esempio, l'interferenza con i recettori M1 centrali mediante l'uso di pirenzepina somministrata direttamente nell'ippocampo ha determinato una compromissione della memoria spaziale in modelli di ratti.[92] Inoltre, è stato osservato che i topi privi del recettore M1 manifestano difetti in vari processi cognitivi,[93] mentre l'uso di agonisti del recettore M1 ha dimostrato di invertire l'impairment dell'apprendimento e della memoria spaziale in modelli animali di malattia di Alzheimer.[94] Studi clinici hanno segnalato che l'impiego di un agonista dei recettori M1/M4 ha migliorato le funzioni cognitive nei pazienti affetti da malattia di Alzheimer, valutate tramite scale di gravità della malattia. Tuttavia, è importante notare che tale trattamento è stato associato a una frequente comparsa di effetti collaterali sistemici.[95] Pertanto, l'antagonismo selettivo dei recettori M1 a livello centrale può comportare disfunzioni cognitive e altri eventi avversi nel SNC. Questi effetti sono sempre più associati agli agenti antimuscarinici con un'elevata affinità per i recettori M1.[96][97][98]
Inoltre, l'attività dei recettori M2 nel SNC potrebbe contribuire anch'essa al deterioramento delle funzioni cognitive, poiché i topi privi di tali recettori mostrano deficit cognitivi.[99] Uno studio successivo ha ulteriormente approfondito queste scoperte, rilevando un deficit nella flessibilità comportamentale, nella memoria di lavoro e nella plasticità dell'ippocampo nei topi privi del recettore M2.[100]
Benché non sia possibile replicare tali studi negli esseri umani, hanno dimostrato che i pazienti affetti da malattia di Parkinson, trattati per oltre 2 anni con agenti antimuscarinici meno selettivi come orfenadrina, ossibutinina e triexifenidile, presentano maggiori segni patologici associati alla malattia di Alzheimer rispetto ai pazienti non trattati con tali agenti.[101] Questi risultati suggeriscono che sia i recettori M1 che i recettori M2 nel SNC svolgano un ruolo funzionale cruciale nelle funzioni cognitive. In contrasto, i topi privi del recettore M3 mostrano un normale funzionamento cognitivo e comportamentale.[102]
È importante sottolineare che l'antagonismo dei recettori muscarinici M1 e M2 nell'encefalo dipende non solo dall'affinità del farmaco per questi recettori, ma anche dalla concentrazione del farmaco all'interno del sistema nervoso centrale (SNC). Ciò è determinato dall'equilibrio tra la penetrazione del farmaco attraverso la barriera emato-encefalica (BEE) e la fuoriuscita dal SNC. Pertanto, la dimensione molecolare, la polarità e la lipofilia, nonché la specificità per la pompa di efflusso della glicoproteina P, possono influenzare il rischio di effetti avversi del SNC con i farmaci antimuscarinici. Tuttavia, i livelli di farmaco nel SNC possono variare in situazioni in cui la BEE diventa "permeabile" a seguito di danni (ad esempio, in condizioni di stress, età avanzata o presenza di patologie comorbide come il diabete o la sclerosi multipla).[103][104][105][106][107][108]
I meccanismi implicati nell'aumento della permeabilità della BEE includono il restringimento dell'epitelio accompagnato dall'apertura delle giunzioni strette e la dilatazione dei vasi sanguigni, che comporta un aumento del flusso sanguigno e del trasporto, come mostrato in un modello di ratto. Altri meccanismi potrebbero includere un'attività pinocitotica potenziata, che si osserva con l'avanzare dell'età. Di conseguenza, tutti gli antagonisti dei recettori antimuscarinici, indipendentemente dalle loro proprietà fisico-chimiche, hanno il potenziale per attraversare la BEE, sebbene il livello di affinità/concentrazione sierica necessario per influenzare i recettori muscarinici che mediano la funzione cognitiva richieda ulteriori indagini. Tuttavia, le evidenze disponibili suggeriscono che una questione chiave per ridurre al minimo eventuali eventi avversi cognitivi con gli agenti antimuscarinici sarebbe il risparmio del recettore M1.[105][109]
Meccanismo d'azione
modificaI recettori muscarinici si trovano negli organi bersaglio del sistema parasimpatico e in alcuni bersagli simpatici, come le ghiandole sudoripare eccrine (che producono abbondante secrezione nella termoregolazione per dissipare il calore) e i vasi sanguigni nei muscoli scheletrici (che vengono dilatati). I recettori muscarinici dell'acetilcolina nel sistema nervoso periferico si trovano principalmente sulle cellule effettori del sistema autonomo innervate dai nervi parasimpatici postgangliari. I recettori muscarinici sono presenti anche nei gangli e su alcune cellule, come le cellule endoteliali dei vasi sanguigni che ricevono poca o nessuna innervazione colinergica. All'interno del sistema nervoso centrale (SNC), l'ippocampo, la corteccia e il talamo presentano alte densità di recettori muscarinici. Inizialmente, gli studi e la ricerca nei confronti dei recettori muscarinici sono stati caratterizzati mediante l'analisi delle risposte di cellule e tessuti periferici e nel SNC. Gli effetti differenziali di due agonisti muscarinici, bethanechol e McN-A-343, sul tono dello sfintere esofageo inferiore hanno portato alla designazione iniziale dei recettori muscarinici come M1 (ganglionico) e M2 (cellula effettore). La base della selettività di questi agonisti è ancora poco chiara, poiché vi sono poche prove che gli agonisti discriminino in modo apprezzabile tra i sottotipi dei recettori muscarinici.[110][111] Tuttavia, successivi studi di legame con radioligandi hanno rivelato definitivamente popolazioni distinte di siti di legame degli antagonisti.[112]
In particolare, una regione nell'estremità carbossiterminale del terzo loop intracellulare del recettore è stata implicata nella specificità dell'accoppiamento con la proteina G e mostra un'ampia omologia tra i recettori M1, M3 e M5 e tra i recettori M2 e M4. Regioni conservate nel secondo loop intracellulare conferiscono anche la specificità per il corretto riconoscimento della proteina G. Sebbene la selettività non sia assoluta, la stimolazione dei recettori M1 o M3 provoca l'idrolisi dei polifosfoinositidi e la mobilizzazione del calcio intracellulare come conseguenza dell'attivazione della via Gq-PLC; questo effetto a sua volta provoca una varietà di eventi mediati dal calcio, direttamente o come conseguenza della fosforilazione di proteine bersaglio. Al contrario, i recettori muscarinici M2 e M4 inibiscono l'adenilato ciclasi e regolano specifici canali ionici (ad esempio, l'aumento della conduttanza del K+ nel tessuto atriale cardiaco) attraverso subunità rilasciate da proteine G sensibili alla tossina del pertosse (Gi e G0) che sono distinte dalle proteine G utilizzate dai recettori M1 e M3.[113] In particolare, l'antagonista muscarinico pirenzepina si è dimostrato legare con alta affinità ai siti nella corteccia cerebrale e nei gangli simpatici (M1), ma con una minore affinità per i siti nel muscolo cardiaco, nel muscolo liscio e in varie ghiandole. Questi dati spiegano la capacità della pirenzepina di bloccare le risposte indotte dall'agonista che sono mediate dai recettori muscarinici nei gangli simpatici e mienterici a concentrazioni considerevolmente inferiori rispetto a quelle richieste per bloccare le risposte che derivano dalla stimolazione diretta dei recettori negli organi effettori vari. Sono ora disponibili antagonisti che possono discriminare ulteriormente tra i diversi sottotipi di recettori muscarinici. Ad esempio, la tripitramina mostra selettività per i recettori muscarinici M2 cardiaci rispetto ai recettori muscarinici M3, mentre la darifenacina è relativamente selettiva nell'antagonizzare i recettori muscarinici M3 delle ghiandole e del muscolo liscio rispetto ai recettori M2.[6][7]
Note
modifica- ^ Megan Kudlak e Prasanna Tadi, Physiology, Muscarinic Receptor, StatPearls Publishing, 2023. URL consultato il 10 giugno 2023.
- ^ a b (EN) Zhong Jin, Muscarine, imidazole, oxazole and thiazole alkaloids, in Natural Product Reports, vol. 33, n. 11, 26 ottobre 2016, pp. 1268–1317, DOI:10.1039/C6NP00067C. URL consultato il 10 giugno 2023.
- ^ Alena A. Kozlova, Michelle Lotfi e Peter G. Okkema, Cross Talk with the GAR-3 Receptor Contributes to Feeding Defects in Caenorhabditis elegans eat-2 Mutants, in Genetics, vol. 212, n. 1, 2019-05, pp. 231–243, DOI:10.1534/genetics.119.302053. URL consultato il 10 giugno 2023.
- ^ Bhavik Patel, Fernando Perez e Patrik Aronsson, Combination drug therapy against OAB normalizes micturition parameters and increases the release of nitric oxide during chemically induced cystitis, in Pharmacology Research & Perspectives, vol. 8, n. 1, 2020-02, pp. e00564, DOI:10.1002/prp2.564. URL consultato il 10 giugno 2023.
- ^ Timothy E. Albertson, James A. Chenoweth e Skyler J. Pearson, The pharmacological management of asthma-chronic obstructive pulmonary disease overlap syndrome (ACOS), in Expert Opinion on Pharmacotherapy, vol. 21, n. 2, 2020-02, pp. 213–231, DOI:10.1080/14656566.2019.1701656. URL consultato il 10 giugno 2023.
- ^ a b (EN) Ritsuko Inoue, Toshihiko Aosaki e Masami Miura, Protein kinase C activity alters the effect of μ-opioid receptors on inhibitory postsynaptic current in the striosomes, in NeuroReport, vol. 23, n. 3, 15 febbraio 2012, pp. 184, DOI:10.1097/WNR.0b013e32834faab0. URL consultato il 10 giugno 2023.
- ^ a b (EN) Prashant Tiwari, Shubhangi Dwivedi e Mukesh Pratap Singh, Basic and modern concepts on cholinergic receptor: A review, in Asian Pacific Journal of Tropical Disease, vol. 3, n. 5, 1º ottobre 2013, pp. 413–420, DOI:10.1016/S2222-1808(13)60094-8. URL consultato il 10 giugno 2023.
- ^ a b CHRM1 cholinergic receptor muscarinic 1 [Homo sapiens (human)] - Gene - NCBI, su ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ a b (EN) PubChem, CHRM1 - cholinergic receptor muscarinic 1 (human), su pubchem.ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ a b c d Linn Fagerberg, Björn M. Hallström e Per Oksvold, Analysis of the human tissue-specific expression by genome-wide integration of transcriptomics and antibody-based proteomics, in Molecular & cellular proteomics: MCP, vol. 13, n. 2, 2014-02, pp. 397–406, DOI:10.1074/mcp.M113.035600. URL consultato il 14 giugno 2023.
- ^ (EN) PubChem, CHRM2 - cholinergic receptor muscarinic 2 (human), su pubchem.ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ CHRM2 cholinergic receptor muscarinic 2 [Homo sapiens (human)] - Gene - NCBI, su ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ CHRM3 cholinergic receptor muscarinic 3 [Homo sapiens (human)] - Gene - NCBI, su ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ Alliance of Genome Resources, su alliancegenome.org. URL consultato il 14 giugno 2023.
- ^ UniProt, su uniprot.org. URL consultato il 14 giugno 2023.
- ^ CHRM4 cholinergic receptor muscarinic 4 [Homo sapiens (human)] - Gene - NCBI, su ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ (EN) PubChem, Muscarinic acetylcholine receptor M4 (human), su pubchem.ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ CHRM5 cholinergic receptor muscarinic 5 [Homo sapiens (human)] - Gene - NCBI, su ncbi.nlm.nih.gov. URL consultato il 14 giugno 2023.
- ^ Alliance of Genome Resources, su alliancegenome.org. URL consultato il 14 giugno 2023.
- ^ a b Tripathi KD (2004). Essentials of Medical Pharmacology (5th ed.). India: Jaypee Brothers, Medical Publishers. pp. 890 pages. ISBN 978-81-8061-187-2. if nothing else mentioned in table
- ^ (EN) Richard S. Smith e Ricardo C. Araneda, Cholinergic Modulation of Neuronal Excitability in the Accessory Olfactory Bulb, in Journal of Neurophysiology, vol. 104, n. 6, 2010-12, pp. 2963–2974, DOI:10.1152/jn.00446.2010. URL consultato il 12 giugno 2023.
- ^ (EN) Alexei V. Egorov, Bassam N. Hamam e Erik Fransén, Graded persistent activity in entorhinal cortex neurons, in Nature, vol. 420, n. 6912, 2002-11, pp. 173–178, DOI:10.1038/nature01171. URL consultato il 12 giugno 2023.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av Pharmacology, 5. ed, Churchill Livingstone, 2003, ISBN 978-0-443-07145-4.
- ^ a b Adlei B. Carlson e Gregory P. Kraus, Physiology, Cholinergic Receptors, StatPearls Publishing, 2023. URL consultato il 12 giugno 2023.
- ^ (EN) Paul Abrams, Karl-Erik Andersson e Jerry J Buccafusco, Muscarinic receptors: their distribution and function in body systems, and the implications for treating overactive bladder: Muscarinic receptors: distribution and function, in British Journal of Pharmacology, vol. 148, n. 5, 2006-07, pp. 565–578, DOI:10.1038/sj.bjp.0706780. URL consultato il 12 giugno 2023.
- ^ a b (EN) C. Ghelardini, N. Galeotti e C. Lelli, M1 receptor activation is a requirement for arecoline analgesia, in Il Farmaco, vol. 56, n. 5, 1º luglio 2001, pp. 383–385, DOI:10.1016/S0014-827X(01)01091-6. URL consultato il 12 giugno 2023.
- ^ (EN) N Uchimura e R A North, Muscarine reduces inwardly rectifying potassium conductance in rat nucleus accumbens neurones., in The Journal of Physiology, vol. 422, n. 1, 1º marzo 1990, pp. 369–380, DOI:10.1113/jphysiol.1990.sp017989. URL consultato il 12 giugno 2023.
- ^ (EN) Jelveh Lameh, Ethan S. Burstein e Eve Taylor, Pharmacology of N-desmethylclozapine, in Pharmacology & Therapeutics, vol. 115, n. 2, 1º agosto 2007, pp. 223–231, DOI:10.1016/j.pharmthera.2007.05.004. URL consultato il 12 giugno 2023.
- ^ (EN) Yoshihisa Kitamura, Toshio Kaneda e Yasuyuki Nomura, Effects of Nebracetam (WEB 1881 FU), a Novel Nootropic, as a Mi-Muscarinic Agonist, in Japanese Journal of Pharmacology, vol. 55, n. 1, 1º gennaio 1991, pp. 177–180, DOI:10.1016/S0021-5198(19)52085-6. URL consultato il 12 giugno 2023.
- ^ Edwards Pharmaceuticals, Inc.; Belcher Pharmaceuticals, Inc. (May 2010). "DailyMed". U.S. National Library of Medicine. Retrieved January 13, 2013.
- ^ a b (EN) Denis Servent, Guillaume Blanchet e Gilles Mourier, Muscarinic toxins, in Toxicon, vol. 58, n. 6, 1º novembre 2011, pp. 455–463, DOI:10.1016/j.toxicon.2011.08.004. URL consultato il 12 giugno 2023.
- ^ a b (EN) Evert Karlsson, Mikael Jolkkonen e Ezra Mulugeta, Snake toxins with high selectivity for subtypesof muscarinic acetylcholine receptors, in Biochimie, vol. 82, n. 9, 10 settembre 2000, pp. 793–806, DOI:10.1016/S0300-9084(00)01176-7. URL consultato il 12 giugno 2023.
- ^ a b c Human Metabolome Database: Showing metabocard for Arecoline (HMDB0030353), su hmdb.ca. URL consultato il 12 giugno 2023.
- ^ a b ED-SPAZ NDC 0485-0082-01 HYOSCYAMINE SULFATE ORALLY DISINTEGRATING TABLETS, 0.125 MG, su dailymed.nlm.nih.gov. URL consultato il 12 giugno 2023.
- ^ M. P. Caulfield e N. J. Birdsall, International Union of Pharmacology. XVII. Classification of muscarinic acetylcholine receptors, in Pharmacological Reviews, vol. 50, n. 2, 1998-06, pp. 279–290. URL consultato l'11 giugno 2023.
- ^ P. Wang, G. R. Luthin e M. R. Ruggieri, Muscarinic acetylcholine receptor subtypes mediating urinary bladder contractility and coupling to GTP binding proteins, in The Journal of Pharmacology and Experimental Therapeutics, vol. 273, n. 2, 1995-05, pp. 959–966. URL consultato l'11 giugno 2023.
- ^ S. S. Hegde e R. M. Eglen, Muscarinic receptor subtypes modulating smooth muscle contractility in the urinary bladder, in Life Sciences, vol. 64, n. 6-7, 1999, pp. 419–428, DOI:10.1016/s0024-3205(98)00581-5. URL consultato l'11 giugno 2023.
- ^ Charlotte Fetscher, Marina Fleichman e Martina Schmidt, M(3) muscarinic receptors mediate contraction of human urinary bladder, in British Journal of Pharmacology, vol. 136, n. 5, 2002-07, pp. 641–643, DOI:10.1038/sj.bjp.0704781. URL consultato l'11 giugno 2023.
- ^ R. Chess-Williams, C. R. Chapple e T. Yamanishi, The minor population of M3-receptors mediate contraction of human detrusor muscle in vitro, in Journal of Autonomic Pharmacology, vol. 21, n. 5-6, 2001, pp. 243–248, DOI:10.1046/j.1365-2680.2001.00231.x. URL consultato l'11 giugno 2023.
- ^ M. Matsui, D. Motomura e H. Karasawa, Multiple functional defects in peripheral autonomic organs in mice lacking muscarinic acetylcholine receptor gene for the M3 subtype, in Proceedings of the National Academy of Sciences of the United States of America, vol. 97, n. 17, 15 agosto 2000, pp. 9579–9584, DOI:10.1073/pnas.97.17.9579. URL consultato l'11 giugno 2023.
- ^ Yasuhiko Igawa, Xiaoyang Zhang e Osamu Nishizawa, Cystometric findings in mice lacking muscarinic M2 or M3 receptors, in The Journal of Urology, vol. 172, 6 Pt 1, 2004-12, pp. 2460–2464, DOI:10.1097/01.ju.0000138054.77785.4a. URL consultato l'11 giugno 2023.
- ^ Frederick J. Ehlert, Michael T. Griffin e Diane M. Abe, The M2 muscarinic receptor mediates contraction through indirect mechanisms in mouse urinary bladder, in The Journal of Pharmacology and Experimental Therapeutics, vol. 313, n. 1, 2005-04, pp. 368–378, DOI:10.1124/jpet.104.077909. URL consultato l'11 giugno 2023.
- ^ S. S. Hegde, A. Choppin e D. Bonhaus, Functional role of M2 and M3 muscarinic receptors in the urinary bladder of rats in vitro and in vivo, in British Journal of Pharmacology, vol. 120, n. 8, 1997-04, pp. 1409–1418, DOI:10.1038/sj.bjp.0701048. URL consultato l'11 giugno 2023.
- ^ a b A. S. Braverman, G. R. Luthin e M. R. Ruggieri, M2 muscarinic receptor contributes to contraction of the denervated rat urinary bladder, in The American Journal of Physiology, vol. 275, n. 5, 1998-11, pp. R1654–1660, DOI:10.1152/ajpregu.1998.275.5.R1654. URL consultato l'11 giugno 2023.
- ^ Alan S. Braverman e Michael R. Ruggieri, Hypertrophy changes the muscarinic receptor subtype mediating bladder contraction from M3 toward M2, in American Journal of Physiology. Regulatory, Integrative and Comparative Physiology, vol. 285, n. 3, 2003-09, pp. R701–708, DOI:10.1152/ajpregu.00009.2003. URL consultato l'11 giugno 2023.
- ^ Michel A. Pontari, Alan S. Braverman e Michael R. Ruggieri, The M2 muscarinic receptor mediates in vitro bladder contractions from patients with neurogenic bladder dysfunction, in American Journal of Physiology. Regulatory, Integrative and Comparative Physiology, vol. 286, n. 5, 2004-05, pp. R874–880, DOI:10.1152/ajpregu.00391.2003. URL consultato l'11 giugno 2023.
- ^ V. P. Krichevsky, M. K. Pagala e I. Vaydovsky, Function of M3 muscarinic receptors in the rat urinary bladder following partial outlet obstruction, in The Journal of Urology, vol. 161, n. 5, 1999-05, pp. 1644–1650. URL consultato l'11 giugno 2023.
- ^ J. A. Gosling, J. S. Dixon e P. Y. Jen, The distribution of noradrenergic nerves in the human lower urinary tract. A review, in European Urology, 36 Suppl 1, 1999, pp. 23–30, DOI:10.1159/000052314. URL consultato l'11 giugno 2023.
- ^ Google Scholar, su scholar.google.com. URL consultato l'11 giugno 2023.
- ^ Google Scholar, su scholar.google.com. URL consultato l'11 giugno 2023.
- ^ Christopher H. Fry, Youko Ikeda e Richard Harvey, Control of bladder function by peripheral nerves: avenues for novel drug targets, in Urology, vol. 63, 3 Suppl 1, 2004-03, pp. 24–31, DOI:10.1016/j.urology.2003.10.031. URL consultato l'11 giugno 2023.
- ^ J. I. Gillespie, The autonomous bladder: a view of the origin of bladder overactivity and sensory urge, in BJU international, vol. 93, n. 4, 2004-03, pp. 478–483, DOI:10.1111/j.1464-410x.2003.04667.x. URL consultato l'11 giugno 2023.
- ^ J. I. Gillespie, Modulation of autonomous contractile activity in the isolated whole bladder of the guinea pig, in BJU international, vol. 93, n. 3, 2004-02, pp. 393–400, DOI:10.1111/j.1464-410x.2003.04624.x. URL consultato l'11 giugno 2023.
- ^ J. I. Gillespie, I. J. Harvey e M. J. Drake, Agonist- and nerve-induced phasic activity in the isolated whole bladder of the guinea pig: evidence for two types of bladder activity, in Experimental Physiology, vol. 88, n. 3, 2003-05, pp. 343–357, DOI:10.1113/eph8802536. URL consultato l'11 giugno 2023.
- ^ Masaki Yoshida, Koichi Miyamae e Hitoshi Iwashita, Management of detrusor dysfunction in the elderly: changes in acetylcholine and adenosine triphosphate release during aging, in Urology, vol. 63, 3 Suppl 1, 2004-03, pp. 17–23, DOI:10.1016/j.urology.2003.11.003. URL consultato l'11 giugno 2023.
- ^ L. A. Birder, S. R. Barrick e J. R. Roppolo, Feline interstitial cystitis results in mechanical hypersensitivity and altered ATP release from bladder urothelium, in American Journal of Physiology. Renal Physiology, vol. 285, n. 3, 2003-09, pp. F423–429, DOI:10.1152/ajprenal.00056.2003. URL consultato l'11 giugno 2023.
- ^ a b R. Chess-Williams, Muscarinic receptors of the urinary bladder: detrusor, urothelial and prejunctional, in Autonomic & Autacoid Pharmacology, vol. 22, n. 3, 2002-06, pp. 133–145, DOI:10.1046/j.1474-8673.2002.00258.x. URL consultato l'11 giugno 2023.
- ^ Hongxia Zhou, Angelika Meyer e Klaus Starke, Heterogeneity of release-inhibiting muscarinic autoreceptors in heart atria and urinary bladder: a study with M(2)- and M(4)-receptor-deficient mice, in Naunyn-Schmiedeberg's Archives of Pharmacology, vol. 365, n. 2, 2002-02, pp. 112–122, DOI:10.1007/s00210-001-0517-7. URL consultato l'11 giugno 2023.
- ^ G. T. Somogyi, M. Tanowitz e G. Zernova, M1 muscarinic receptor-induced facilitation of ACh and noradrenaline release in the rat bladder is mediated by protein kinase C, in The Journal of Physiology, 496 ( Pt 1), Pt 1, 1º ottobre 1996, pp. 245–254, DOI:10.1113/jphysiol.1996.sp021681. URL consultato l'11 giugno 2023.
- ^ G. T. Somogyi e W. C. de Groat, Function, signal transduction mechanisms and plasticity of presynaptic muscarinic receptors in the urinary bladder, in Life Sciences, vol. 64, n. 6-7, 1999, pp. 411–418, DOI:10.1016/s0024-3205(98)00580-3. URL consultato l'11 giugno 2023.
- ^ George T. Somogyi, Ganna V. Zernova e Mitsuharu Yoshiyama, Change in muscarinic modulation of transmitter release in the rat urinary bladder after spinal cord injury, in Neurochemistry International, vol. 43, n. 1, 2003-07, pp. 73–77, DOI:10.1016/s0197-0186(02)00193-6. URL consultato l'11 giugno 2023.
- ^ C. R. Chapple, Muscarinic receptor antagonists in the treatment of overactive bladder, in Urology, vol. 55, 5A Suppl, 2000-05, pp. 33–46; discussion 50, DOI:10.1016/s0090-4295(99)00492-6. URL consultato l'11 giugno 2023.
- ^ B. J. Baum, Principles of saliva secretion, in Annals of the New York Academy of Sciences, vol. 694, 20 settembre 1993, pp. 17–23, DOI:10.1111/j.1749-6632.1993.tb18338.x. URL consultato l'11 giugno 2023.
- ^ D. J. Culp, W. Luo e L. A. Richardson, Both M1 and M3 receptors regulate exocrine secretion by mucous acini, in The American Journal of Physiology, vol. 271, 6 Pt 1, 1996-12, pp. C1963–1972, DOI:10.1152/ajpcell.1996.271.6.C1963. URL consultato l'11 giugno 2023.
- ^ E. L. Watson, P. W. Abel e D. DiJulio, Identification of muscarinic receptor subtypes in mouse parotid gland, in The American Journal of Physiology, vol. 271, 3 Pt 1, 1996-09, pp. C905–913, DOI:10.1152/ajpcell.1996.271.3.C905. URL consultato l'11 giugno 2023.
- ^ Dimitra Beroukas, Rhian Goodfellow e Jenny Hiscock, Up-regulation of M3-muscarinic receptors in labial salivary gland acini in primary Sjögren's syndrome, in Laboratory Investigation; a Journal of Technical Methods and Pathology, vol. 82, n. 2, 2002-02, pp. 203–210, DOI:10.1038/labinvest.3780412. URL consultato l'11 giugno 2023.
- ^ Gunnar Tobin, Daniel Giglio e Bengt Götrick, Studies of muscarinic receptor subtypes in salivary gland function in anaesthetized rats, in Autonomic Neuroscience: Basic & Clinical, vol. 100, n. 1-2, 30 settembre 2002, pp. 1–9, DOI:10.1016/s1566-0702(02)00139-x. URL consultato l'11 giugno 2023.
- ^ a b c Frank P. Bymaster, Petra A. Carter e Masahisa Yamada, Role of specific muscarinic receptor subtypes in cholinergic parasympathomimetic responses, in vivo phosphoinositide hydrolysis, and pilocarpine-induced seizure activity, in The European Journal of Neuroscience, vol. 17, n. 7, 2003-04, pp. 1403–1410, DOI:10.1046/j.1460-9568.2003.02588.x. URL consultato l'11 giugno 2023.
- ^ a b Dinesh Gautam, Thomas S. Heard e Yinghong Cui, Cholinergic stimulation of salivary secretion studied with M1 and M3 muscarinic receptor single- and double-knockout mice, in Molecular Pharmacology, vol. 66, n. 2, 2004-08, pp. 260–267, DOI:10.1124/mol.66.2.260. URL consultato l'11 giugno 2023.
- ^ P. G. Gillberg, S. Sundquist e L. Nilvebrant, Comparison of the in vitro and in vivo profiles of tolterodine with those of subtype-selective muscarinic receptor antagonists, in European Journal of Pharmacology, vol. 349, n. 2-3, 22 maggio 1998, pp. 285–292, DOI:10.1016/s0014-2999(98)00214-3. URL consultato l'11 giugno 2023.
- ^ Ken Ikeda, Seiji Kobayashi e Mami Suzuki, M(3) receptor antagonism by the novel antimuscarinic agent solifenacin in the urinary bladder and salivary gland, in Naunyn-Schmiedeberg's Archives of Pharmacology, vol. 366, n. 2, 2002-08, pp. 97–103, DOI:10.1007/s00210-002-0554-x. URL consultato l'11 giugno 2023.
- ^ a b c d M. Matsui, D. Motomura e H. Karasawa, Multiple functional defects in peripheral autonomic organs in mice lacking muscarinic acetylcholine receptor gene for the M3 subtype, in Proceedings of the National Academy of Sciences of the United States of America, vol. 97, n. 17, 15 agosto 2000, pp. 9579–9584, DOI:10.1073/pnas.97.17.9579. URL consultato l'11 giugno 2023.
- ^ W. Luo, L. R. Latchney e D. J. Culp, G protein coupling to M1 and M3 muscarinic receptors in sublingual glands, in American Journal of Physiology. Cell Physiology, vol. 280, n. 4, 2001-04, pp. C884–896, DOI:10.1152/ajpcell.2001.280.4.C884. URL consultato l'11 giugno 2023.
- ^ Gunnar Tobin, Presynaptic muscarinic receptor mechanisms and submandibular responses to stimulation of the parasympathetic innervation in bursts in rats, in Autonomic Neuroscience: Basic & Clinical, vol. 99, n. 2, 30 agosto 2002, pp. 111–118, DOI:10.1016/s1566-0702(02)00094-2. URL consultato l'11 giugno 2023.
- ^ Ananias C. Diokno, Rodney A. Appell e Peter K. Sand, Prospective, randomized, double-blind study of the efficacy and tolerability of the extended-release formulations of oxybutynin and tolterodine for overactive bladder: results of the OPERA trial, in Mayo Clinic Proceedings, vol. 78, n. 6, 2003-06, pp. 687–695, DOI:10.4065/78.6.687. URL consultato l'11 giugno 2023.
- ^ F. Haab, L. Stewart e P. Dwyer, Darifenacin, an M3 selective receptor antagonist, is an effective and well-tolerated once-daily treatment for overactive bladder, in European Urology, vol. 45, n. 4, 2004-04, pp. 420–429; discussion 429, DOI:10.1016/j.eururo.2004.01.008. URL consultato l'11 giugno 2023.
- ^ Robert B. Armstrong, Karl M. Luber e Kenneth M. Peters, Comparison of dry mouth in women treated with extended-release formulations of oxybutynin or tolterodine for overactive bladder, in International Urology and Nephrology, vol. 37, n. 2, 2005, pp. 247–252, DOI:10.1007/s11255-004-4703-7. URL consultato l'11 giugno 2023.
- ^ C. R. Chapple e P. Abrams, Comparison of darifenacin and oxybutynin in patients with overactive bladder: assessment of ambulatory urodynamics and impact on salivary flow, in European Urology, vol. 48, n. 1, 2005-07, pp. 102–109, DOI:10.1016/j.eururo.2005.04.018. URL consultato l'11 giugno 2023.
- ^ a b Christopher Chapple, William Steers e Peggy Norton, A pooled analysis of three phase III studies to investigate the efficacy, tolerability and safety of darifenacin, a muscarinic M3 selective receptor antagonist, in the treatment of overactive bladder, in BJU international, vol. 95, n. 7, 2005-05, pp. 993–1001, DOI:10.1111/j.1464-410X.2005.05454.x. URL consultato l'11 giugno 2023.
- ^ Insuk So, Dong Ki Yang e Hyun Jin Kim, Five subtypes of muscarinic receptors are expressed in gastric smooth muscles of guinea pig, in Experimental & Molecular Medicine, vol. 35, n. 1, 28 febbraio 2003, pp. 46–52, DOI:10.1038/emm.2003.7. URL consultato l'11 giugno 2023.
- ^ A. Gómez, F. Martos e I. Bellido, Muscarinic receptor subtypes in human and rat colon smooth muscle, in Biochemical Pharmacology, vol. 43, n. 11, 9 giugno 1992, pp. 2413–2419, DOI:10.1016/0006-2952(92)90321-9. URL consultato l'11 giugno 2023.
- ^ P. M. Kerr, K. Hillier e R. M. Wallis, Characterization of muscarinic receptors mediating contractions of circular and longitudinal muscle of human isolated colon, in British Journal of Pharmacology, vol. 115, n. 8, 1995-08, pp. 1518–1524, DOI:10.1111/j.1476-5381.1995.tb16645.x. URL consultato l'11 giugno 2023.
- ^ R. M. Eglen e G. C. Harris, Selective inactivation of muscarinic M2 and M3 receptors in guinea-pig ileum and atria in vitro, in British Journal of Pharmacology, vol. 109, n. 4, 1993-08, pp. 946–952, DOI:10.1111/j.1476-5381.1993.tb13712.x. URL consultato l'11 giugno 2023.
- ^ T. Chiba, A. E. Bharucha e G. M. Thomforde, Model of rapid gastrointestinal transit in dogs: effects of muscarinic antagonists and a nitric oxide synthase inhibitor, in Neurogastroenterology and Motility: The Official Journal of the European Gastrointestinal Motility Society, vol. 14, n. 5, 2002-10, pp. 535–541, DOI:10.1046/j.1365-2982.2002.00357.x. URL consultato l'11 giugno 2023.
- ^ Mona Li, Christopher P. Johnson e Mark B. Adams, Cholinergic and nitrergic regulation of in vivo giant migrating contractions in rat colon, in American Journal of Physiology. Gastrointestinal and Liver Physiology, vol. 283, n. 3, 2002-09, pp. G544–552, DOI:10.1152/ajpgi.00114.2001. URL consultato l'11 giugno 2023.
- ^ Minoru Matsui, Daisuke Motomura e Toru Fujikawa, Mice lacking M2 and M3 muscarinic acetylcholine receptors are devoid of cholinergic smooth muscle contractions but still viable, in The Journal of Neuroscience: The Official Journal of the Society for Neuroscience, vol. 22, n. 24, 15 dicembre 2002, pp. 10627–10632, DOI:10.1523/JNEUROSCI.22-24-10627.2002. URL consultato l'11 giugno 2023.
- ^ R. M. Eglen, Muscarinic receptors and gastrointestinal tract smooth muscle function, in Life Sciences, vol. 68, n. 22-23, 27 aprile 2001, pp. 2573–2578, DOI:10.1016/s0024-3205(01)01054-2. URL consultato l'11 giugno 2023.
- ^ Michael D. Gershon, Serotonin and its implication for the management of irritable bowel syndrome, in Reviews in Gastroenterological Disorders, 3 Suppl 2, 2003, pp. S25–34. URL consultato l'11 giugno 2023.
- ^ Google Scholar, su scholar.google.com. URL consultato l'11 giugno 2023.
- ^ Laura A. Volpicelli e Allan I. Levey, Muscarinic acetylcholine receptor subtypes in cerebral cortex and hippocampus, in Progress in Brain Research, vol. 145, 2004, pp. 59–66, DOI:10.1016/S0079-6123(03)45003-6. URL consultato l'11 giugno 2023.
- ^ Table 1: Location of muscarinic receptors in the brain, su ncbi.nlm.nih.gov.
- ^ W. S. Messer, M. Bohnett e J. Stibbe, Evidence for a preferential involvement of M1 muscarinic receptors in representational memory, in Neuroscience Letters, vol. 116, n. 1-2, 14 agosto 1990, pp. 184–189, DOI:10.1016/0304-3940(90)90407-z. URL consultato l'11 giugno 2023.
- ^ Stephan G. Anagnostaras, Geoffrey G. Murphy e Susan E. Hamilton, Selective cognitive dysfunction in acetylcholine M1 muscarinic receptor mutant mice, in Nature Neuroscience, vol. 6, n. 1, 2003-01, pp. 51–58, DOI:10.1038/nn992. URL consultato l'11 giugno 2023.
- ^ Abraham Fisher, Zipora Pittel e Rachel Haring, M1 muscarinic agonists can modulate some of the hallmarks in Alzheimer's disease: implications in future therapy, in Journal of molecular neuroscience: MN, vol. 20, n. 3, 2003, pp. 349–356, DOI:10.1385/JMN:20:3:349. URL consultato l'11 giugno 2023.
- ^ N. C. Bodick, W. W. Offen e A. I. Levey, Effects of xanomeline, a selective muscarinic receptor agonist, on cognitive function and behavioral symptoms in Alzheimer disease, in Archives of Neurology, vol. 54, n. 4, 1997-04, pp. 465–473, DOI:10.1001/archneur.1997.00550160091022. URL consultato l'11 giugno 2023.
- ^ C. A. Donnellan, L. Fook e P. McDonald, Oxybutynin and cognitive dysfunction, in BMJ (Clinical research ed.), vol. 315, n. 7119, 22 novembre 1997, pp. 1363–1364, DOI:10.1136/bmj.315.7119.1363. URL consultato l'11 giugno 2023.
- ^ I. R. Katz, L. P. Sands e W. Bilker, Identification of medications that cause cognitive impairment in older people: the case of oxybutynin chloride, in Journal of the American Geriatrics Society, vol. 46, n. 1, 1998-01, pp. 8–13, DOI:10.1111/j.1532-5415.1998.tb01006.x. URL consultato l'11 giugno 2023.
- ^ Kyle B. Womack e Kenneth M. Heilman, Tolterodine and memory: dry but forgetful, in Archives of Neurology, vol. 60, n. 5, 2003-05, pp. 771–773, DOI:10.1001/archneur.60.5.771. URL consultato l'11 giugno 2023.
- ^ E. T. Tzavara, F. P. Bymaster e C. C. Felder, Dysregulated hippocampal acetylcholine neurotransmission and impaired cognition in M2, M4 and M2/M4 muscarinic receptor knockout mice, in Molecular Psychiatry, vol. 8, n. 7, 2003-07, pp. 673–679, DOI:10.1038/sj.mp.4001270. URL consultato l'11 giugno 2023.
- ^ Thomas Seeger, Irina Fedorova e Fang Zheng, M2 muscarinic acetylcholine receptor knock-out mice show deficits in behavioral flexibility, working memory, and hippocampal plasticity, in The Journal of Neuroscience: The Official Journal of the Society for Neuroscience, vol. 24, n. 45, 10 novembre 2004, pp. 10117–10127, DOI:10.1523/JNEUROSCI.3581-04.2004. URL consultato l'11 giugno 2023.
- ^ Elaine K. Perry, Linda Kilford e Andrew J. Lees, Increased Alzheimer pathology in Parkinson's disease related to antimuscarinic drugs, in Annals of Neurology, vol. 54, n. 2, 2003-08, pp. 235–238, DOI:10.1002/ana.10639. URL consultato l'11 giugno 2023.
- ^ M. Yamada, T. Miyakawa e A. Duttaroy, Mice lacking the M3 muscarinic acetylcholine receptor are hypophagic and lean, in Nature, vol. 410, n. 6825, 8 marzo 2001, pp. 207–212, DOI:10.1038/35065604. URL consultato l'11 giugno 2023.
- ^ R. Liebsch, M. E. Kornhuber e D. Dietl, Blood-CSF barrier integrity in multiple sclerosis, in Acta Neurologica Scandinavica, vol. 94, n. 6, 1996-12, pp. 404–410, DOI:10.1111/j.1600-0404.1996.tb00052.x. URL consultato l'11 giugno 2023.
- ^ M. D. Habgood, D. J. Begley e N. J. Abbott, Determinants of passive drug entry into the central nervous system, in Cellular and Molecular Neurobiology, vol. 20, n. 2, 2000-04, pp. 231–253, DOI:10.1023/a:1007001923498. URL consultato l'11 giugno 2023.
- ^ a b C. Pakulski, L. Drobnik e B. Millo, Age and sex as factors modifying the function of the blood-cerebrospinal fluid barrier, in Medical Science Monitor: International Medical Journal of Experimental and Clinical Research, vol. 6, n. 2, 2000, pp. 314–318. URL consultato l'11 giugno 2023.
- ^ P. Esposito, D. Gheorghe e K. Kandere, Acute stress increases permeability of the blood-brain-barrier through activation of brain mast cells, in Brain Research, vol. 888, n. 1, 5 gennaio 2001, pp. 117–127, DOI:10.1016/s0006-8993(00)03026-2. URL consultato l'11 giugno 2023.
- ^ J. M. Starr, J. Wardlaw e K. Ferguson, Increased blood-brain barrier permeability in type II diabetes demonstrated by gadolinium magnetic resonance imaging, in Journal of Neurology, Neurosurgery, and Psychiatry, vol. 74, n. 1, 2003-01, pp. 70–76, DOI:10.1136/jnnp.74.1.70. URL consultato l'11 giugno 2023.
- ^ Praveen Ballabh, Alex Braun e Maiken Nedergaard, The blood-brain barrier: an overview: structure, regulation, and clinical implications, in Neurobiology of Disease, vol. 16, n. 1, 2004-06, pp. 1–13, DOI:10.1016/j.nbd.2003.12.016. URL consultato l'11 giugno 2023.
- ^ Ali Abdel-Rahman, Ashok K. Shetty e Mohamed B. Abou-Donia, Disruption of the blood-brain barrier and neuronal cell death in cingulate cortex, dentate gyrus, thalamus, and hypothalamus in a rat model of Gulf-War syndrome, in Neurobiology of Disease, vol. 10, n. 3, 2002-08, pp. 306–326, DOI:10.1006/nbdi.2002.0524. URL consultato l'11 giugno 2023.
- ^ (EN) Osamu Ikehara, Hisayoshi Hayashi e Toshiharu Waguri, Subepithelial trypsin induces enteric nerve-mediated anion secretion by activating proteinase-activated receptor 1 in the mouse cecum, in The Journal of Physiological Sciences, vol. 62, n. 3, 2012-05, pp. 211–219, DOI:10.1007/s12576-012-0198-7. URL consultato il 10 giugno 2023.
- ^ Hee Jung Kwon e Hye Young Kim, A Pharmacologic Pupillary Test in the Diagnosis of Diabetic Autonomic Neuropathy, in Korean Journal of Ophthalmology, vol. 23, n. 4, 2009, pp. 291, DOI:10.3341/kjo.2009.23.4.291. URL consultato il 10 giugno 2023.
- ^ (EN) R. J. McLaughlin, M. N. Hill e S. S. Dang, Upregulation of CB1 receptor binding in the ventromedial prefrontal cortex promotes proactive stress-coping strategies following chronic stress exposure, in Behavioural Brain Research, vol. 237, 15 gennaio 2013, pp. 333–337, DOI:10.1016/j.bbr.2012.09.053. URL consultato il 10 giugno 2023.
- ^ (EN) Veli-Pekka Jaakola, Minna Vainio e Saurabh Sen, Intracellularly Truncated Human α 2 B -Adrenoceptors: Stable and Functional GPCRs for Structural Studies, in Journal of Receptors and Signal Transduction, vol. 25, n. 2, 2005-01, pp. 99–124, DOI:10.1081/RRS-200068745. URL consultato il 10 giugno 2023.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su Recettore muscarinico
Collegamenti esterni
modifica- (EN) muscarinic receptor, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.