1,2,3-triazolo
Il 1,2,3-triazolo è uno dei due composti eterociclici aromatici isomeri di formula C2H3N3, detti triazoli, che hanno un anello a cinque termini con due atomi di carbonio e tre atomi di azoto. L'altro isomero è il 1,2,4-triazolo.[1] Il 1,2,3-triazolo è usato nell'ambito della ricerca per costruire composti chimici più complessi, ad esempio farmaci tipo il tazobactam.
| 1,2,3-triazolo | |
|---|---|
 | |
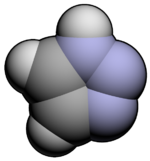 | |
| Nome IUPAC | |
| 1H-1,2,3-triazolo | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H3N3 |
| Massa molecolare (u) | 69,07 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 608-262-3 |
| PubChem | 67516 |
| SMILES | C1=NNN=C1 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,192 |
| Costante di dissociazione acida a K | 6,3 x 10–2 |
| Costante di dissociazione basica a K | 3,98 x 10–10 |
| Solubilità in acqua | molto solubile |
| Temperatura di fusione | 23-25 °C (296-298 K) |
| Temperatura di ebollizione | 203 °C (476 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| Frasi H | 315-319-335 |
| Consigli P | 261-305+351+338 |
Sintesi
modificaGli 1,2,3-triazoli sostituiti si possono produrre tramite la cicloaddizione di Huisgen azide-alchino, dove una azide e un alchino danno luogo ad una ciclizzazione 1,3-dipolare.
Proprietà
modificaIl 1,2,3-triazolo in condizioni normali è un liquido incolore. Esistono due forme tautomere, 1H e 2H. In fase liquida predomina la forma 2H nella maggior parte dei solventi.[2]
La molecola del 1,2,3-triazolo è sorprendentemente stabile rispetto ad altri composti organici contenenti tre atomi di azoto adiacenti. Tuttavia per pirolisi a 500 °C si ha perdita di una molecola di azoto (N2) e formazione di aziridina. Per riscaldamento in opportuni solventi si ha apertura dell'anello e successiva richiusura formando un isomero differente (riarrangiamento di Dimroth).
Indicazioni di sicurezza
modificaIl composto è disponibile in commercio. È irritante per gli occhi, la pelle e le vie respiratorie. Non ci sono dati che indichino proprietà cancerogene. È considerato poco pericoloso per l'ambiente.[3]
Note
modifica- ^ Gilchrist 1987.
- ^ Eicher et al. 2003.
- ^ Alfa Aesar, Scheda di dati di sicurezza del 1,2,3-triazolo (PDF), su alfa.com. URL consultato il 19 novembre 2011.
Bibliografia
modifica- T. Eicher, S. Hauptmann, A. Speicher, 1,2,3-Triazole, in The chemistry of heterocycles: structure, reactions, syntheses, and applications, 2003, p. 201, ISBN 978-3-527-30720-3.
- T. L. Gilchrist, Heterocyclic Chemistry, Prentice Hall, 1987, ISBN 978-0-582-01421-3.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su 1,2,3-triazolo