Dietilpirocarbonato
Il dietilpirocarbonato (DEPC) è usato nei laboratori di biologia molecolare per inattivare le RNAsi eventualmente presenti nell'acqua e sugli strumenti. Agisce legandosi ai residui di istidina, lisina, cisteina e tirosina[2][3][4].
| Dietilpirocarbonato | |
|---|---|
 | |
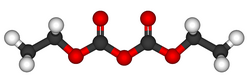 | |
| Nome IUPAC | |
| dicarbonato di dietile | |
| Nomi alternativi | |
| DEPC | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H10O5 |
| Massa molecolare (u) | 162,141 |
| Numero CAS | |
| Numero EINECS | 216-542-8 |
| PubChem | 3051 |
| SMILES | CCOC(=O)OC(=O)OCC |
| Proprietà chimico-fisiche | |
| Temperatura di ebollizione | 93-94 °C a 24 hPa |
| Indicazioni di sicurezza | |
| Punto di fiamma | 69 °C (vaso chiuso) |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 - 315 - 319 - 335 |
| Consigli P | 261 - 305+351+338 [1] |
L'acqua trattata con DEPC (e quindi esente da RNAsi) riduce il rischio che l'RNA possa venire degradato da tracce di RNAsi durante le operazioni di laboratorio.
L'acqua è generalmente trattata con lo 0,1% v/v di DEPC per almeno due ore a 37 °C e quindi passata per almeno 15 minuti in autoclave per eliminare le tracce di DEPC non reagito. Il trattamento in autoclave idrolizza il DEPC in anidride carbonica, acqua ed etanolo. Benché concentrazioni maggiori di DEPC possano eliminare maggiori quantità di RNAsi, non si utilizzano quantità elevate di DEPC perché il DEPC e i suoi sottoprodotti potrebbero successivamente inibire alcune reazioni biochimiche in vitro o promuovere reazioni di carbossimetilazione a danno del campione di RNA.

Il DEPC è instabile in acqua e subisce idrolisi, soprattutto in presenza di specie nucleofile. Per questo motivo il DEPC non può essere usato con i tamponi Tris e HEPES. Può invece essere usato con tamponi fosfato salini e MOPS[5]. Una regola mnemonica è che non è possibile eliminare le RNAsi con DEPC da enzimi e prodotti chimici aventi atomi di -O:, -N: o -S: attivi, perché il DEPC reagisce prima con queste specie.
La reazione di derivatizzazione dei residui di istidina con DEPC è anche usata per studiare il ruolo dei residui di istidina negli enzimi. La reazione dell'istidina con DEPC produce derivati carbossietilati all'azoto imidazolico. Queste reazioni sono reversibili per trattamento con idrossilammina 0,5 M a pH neutro.
Note
modifica- ^ Sigma Aldrich; rev. del 17.06.2014
- ^ Narumi e et al, Neurochem Res., vol. 12, n. 4, 1987.
- ^ Chirgwin, John M, et al., Isolation of biologically active ribonucleic acid from sourcesenriched in ribonuclease, in Biochemistry, vol. 18, n. 24, 1979, pp. 5294–5299, DOI:10.1021/bi00591a005, PMID 518835.
- ^ Barry Wolf, Judith A. Lesnaw e Manfred E. Reichmann, A Mechanism of the Irreversible Inactivation of Bovine Pancreatic Ribonuclease by Diethylpyrocarbonate. A General Reaction of Diethylpyrocarbonate with Proteins, in European Journal of Biochemistry, vol. 13, n. 3, 1970, pp. 519–25, DOI:10.1111/j.1432-1033.1970.tb00955.x, PMID 5444158.
- ^ FAQ about DEPC [collegamento interrotto], su sigma-aldrich.custhelp.com, Sigma-Aldrich. URL consultato il 12 agosto 2012.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su Dietilpirocarbonato