Mola idatiforme
La mola idatiforme (conosciuta anche come mola vescicolare o mola idatidea o mola idatidosa) oppure gravidanza molare, è una forma anomala di gravidanza in cui un ovulo fecondato non vitale si impianta nell'utero e comporta l'instaurarsi di una gravidanza anormale (che non riuscirà ad essere portata a termine).[1]
| Mola idatiforme | |
|---|---|
 | |
| Specialità | patologia |
| Classificazione e risorse esterne (EN) | |
| ICD-O | 9100/0 |
| OMIM | 231090 |
| MeSH | D006828 |
| MedlinePlus | 000909 |
| eMedicine | 254657 e 279116 |
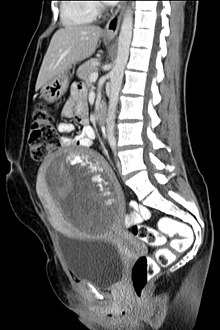
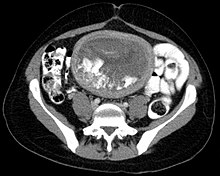
Una gravidanza molare è una malattia gestazionale trofoblastica, ovvero si manifesta in una crescita abnorme del trofoblasto che determina lo svilupparsi di una massa in utero. Questa massa si forma a seguito del rigonfiamento di villi coriali, che si accrescono in gruppi e strutture cistiche che assomigliano a grappoli rigonfi di liquido.
Una gravidanza molare può svilupparsi quando un ovulo privo di nucleo viene fecondato. Quest'ovulo non è poi in grado di convertirsi a tessuto fetale.
Le gravidanze molari sono suddivise in parziali e complete.
Il termine mola, per come viene usato in questo contesto, indica semplicemente una "crescita" di tessuto.
Una mola completa è causata dalla penetrazione di un singolo spermatozoo (90% dei casi) oppure di due spermatozoi (restante 10% della casistica) all'interno di un ovulo che ha perso il suo DNA (lo spermatozoo poi si duplica formando un set "completo" di 46 cromosomi).[2]
Il genotipo è tipicamente 46, XX (diploide) a seguito di successiva mitosi dello spermatozoo fecondante, ma può essere anche 46, XY (diploide).[3] Il genotipo 46, YY (diploide) non è stato mai osservato.
Al contrario, una mola parziale si verifica quando un ovulo normale viene fecondato da due spermatozoi o da uno spermatozoo che duplica se stesso dando luogo ai genotipi 69, XXY (triploide) o 92, XXXY (tetraploide).
Una mola idatiforme completa presenta un rischio più elevato di evolvere in coriocarcinoma - un tumore maligno delle cellule del trofoblasto - rispetto ad una mola parziale.
Una mola idatiforme può essere considerata come un "mancato aborto spontaneo" in quanto la gravidanza è divenuta non vitale ma il prodotto del concepimento non è stato espulso, cioè abortito.[4]
Etimologia
modificaIl termine deriva dal greco hydatís-ídos (che sta a significare "una goccia d'acqua"), con riferimento al contenuto acquoso delle cisti, e dalla lingua latina mole (ovvero masso, riferendosi al falso concepimento). Il termine, secondo altri, deriva dalla somiglianza esistente tra la mola vescicolare e le cisti idatidee proprie dell'echinococcosi.
Epidemiologia
modificaLa mola idatiforme è una complicanza comune della gravidanza, che negli Stati Uniti e nella maggior parte dei paesi si verifica con un'incidenza di circa 1 ogni 1000 gravidanze.[5] In altri paesi, ed in particolare nel continente asiatico, si registrano tassi molto più alti (ad esempio, in Indonesia, fino a 1 caso ogni 100 gravidanze).
In Europa l'incidenza è leggermente più bassa rispetto agli Stati Uniti, e nel nord Italia (nel periodo 1979-1982) è ammontata a 62 casi ogni 100.000 gravidanze.[6]
Gli studi epidemiologici evidenziano che la gravidanza molare è molto più comune agli estremi d'età: le donne con meno di 20 anni od al di sopra dei 40 presentano infatti un rischio maggiore.[7]
Quando una donna ha già avuto una mola idatiforme la probabilità di avere un'ulteriore successiva gravidanza molare è pari a circa l'1-2%.[8][9]
Eziologia
modificaL'eziologia di questa condizione non è completamente nota. I potenziali fattori di rischio possono includere difetti dell'ovulo, anomalie all'interno dell'utero, oppure carenze nutrizionali. Altri fattori di rischio verosimilmente includono le diete a basso contenuto di proteine, vitamina B12, acido folico[10][11] e carotene.[12] In letteratura medica è stato segnalato che anche elevati livelli plasmatici di omocisteina potrebbero giocare un ruolo nello sviluppo del disturbo.[10]
Storia naturale
modificaUna mola idatiforme è una gravidanza, una forma di concepimento, nella quale la placenta si caratterizza per il contenere delle vescicole simili ad acini d'uva, solitamente visibili ad occhio nudo. Le vescicole derivano dalla distensione dei villi coriali ad opera del fluido. Quando il tessuto viene ispezionato al microscopio, balza all'occhio l'iperplasia del tessuto trofoblastico.[13][14] Se non trattata, una mola idatiforme evolverà quasi sempre in un aborto spontaneo (interruzione di gravidanza). Sulla base dell'aspetto morfologico, una mola idatiforme può essere suddivisa in due tipi:
- mola completa - tutti i villi coriali hanno un aspetto vescicolare e non è presente alcun segno di sviluppo embrionale o fetale.
- mola parziale - solo alcuni villi presentano un aspetto vescicolare mentre altri appaiono pressoché normali, ed è possibile apprezzare uno sviluppo embrionale/fetale, ma il feto appare sempre chiaramente malformato e non è possibile che sia vitale.
La diagnosi differenziale tra mola completa ed incompleta si avvale dell'immunoistochimica, tramite ricerca della proteina p57, che viene fisiologicamente inattivata nel genoma paterno. Se tale proteina non viene espressa, vuol dire che tutto il patrimonio genetico è paterno (mola completa).
In rari casi, una mola idatiforme coesiste in utero con un feto normale e vitale. Questi casi sono dovuti al fenomeno dei gemelli. L'utero contiene due prodotti del concepimento: uno con una placenta anomala e nessun feto vitale (la mola idatiforme), e uno con una placenta normale e un feto vitale. Se mantenuta sotto attento controllo medico è spesso possibile per la donna gravida riuscire a dare alla luce il bambino normale e contemporaneamente ricevere un trattamento adeguato per la gravidanza molare.[15]
Il set diploide di DNA proveniente dai soli spermatozoi sta a significare che tutti i cromosomi hanno una soppressione dei geni modellata sullo schema dello spermatozoo ed ottenuta tramite metilazione. Questo fatto porta alla crescita eccessiva del sinciziotrofoblasto mentre la metilazione dell'ovocellula conduce ad una predilezione nell'utilizzo delle risorse a favore dell'embrione, con un sinciziotrofoblasto sottosviluppato. Questo fenomeno si ritiene sia il risultato di una competizione evolutiva con i geni maschili che portano ad investire un gran numero di risorse a favore del feto, mentre i geni femminili indirizzano verso una restrizione delle risorse volta a massimizzare il numero della prole.[16]
Origine parentale
modificaNella maggior parte delle mole complete, tutti i geni del nucleo vengono ereditati solo dal padre (androgenesi). Il meccanismo più probabile e che dà conto di circa l'80% di queste mole androgenetiche è che la cellula uovo vuota (priva di nucleo) sia fecondata da uno spermatozoo, e successivamente si verifichi una duplicazione di tutti i cromosomi e geni (un processo chiamato "endoriduplicazione").
Nel restante 20% delle mole complete, il meccanismo più probabile è che una cellula uovo vuota (priva di nucleo) venga fecondata da due spermatozoi.
In entrambi i casi, le mole sono diploidi (cioè nelle cellule vi è la presenza di due copie di ogni cromosoma).
In tutti questi casi, i geni mitocondriali sono ereditati dalla madre, come al solito.[17]
La maggior parte delle mole parziali sono invece triploidi (tre set cromosomici). Il nucleo contiene un set di geni materni e due set di geni paterni.
Il meccanismo, anche in questo caso, è di solito il raddoppio del set aploide paterno derivante da un unico spermatozoo, ma può anche essere la conseguenza di una fecondazione dell'ovocellula da parte di due spermatozoi.
In rari casi, le mole idatiformi sono tetraploidi (possiedono quattro set di cromosomi) o hanno altre anomalie cromosomiche.[18]
Una piccola percentuale di moli idatidiformi presenta genomi diploidi biparentali, come nelle persone normali in vita. Presenta cioè due set di cromosomi, ciascuno ereditato da ogni genitore biologico. Alcune di queste moli si verificano in donne che presentano mutazioni nel gene NLRP7. Questa mutazione sembra predisporre verso una gravidanza molare. Queste rare varianti di mola idatiforme possono essere complete o parziali.[19][20][21]
Presentazione clinica
modificaLe gravidanze molari di solito esordiscono con sanguinamento vaginale indolore nel quarto-quinto mese di gravidanza.[22][23] L'utero può essere più grande del previsto, oppure le ovaie possono essere ingrandite. Alcune donne accusano vomito estremamente intenso (iperemesi); talvolta vi è un aumento della pressione arteriosa e presenza di proteine nelle urine (proteinuria): questo è il fenomeno della preeclampsia o gestosi (in questo caso gestosi bisintomatica di tipo PH). La mola produce hCG in eccesso rispetto ad una gravidanza normale e gli esami del sangue mostrano concentrazioni estremamente elevate di gonadotropina corionica.[24] Talvolta le donne con mola idatiforme accusano sintomi tipici di ipertiroidismo. Questa sintomatologia è una conseguenza diretta dei livelli estremamente elevati di hCG; questo ormone può infatti mimare l'azione dell'ormone stimolante la tiroide, il TSH, comportandosi dunque come un debole agonista dei recettori della tireotropina (TSH).[25] In questi soggetti, le concentrazioni estremamente elevate di gonadotropina corionica (hCG) ed i livelli soppressi di tireotropina suggeriscono e confermano l'attività tireotropica di hCG.[26][27]
Diagnosi
modificaLa diagnosi è fortemente suggerita dalla semplice esecuzione di un esame ad ultrasuoni (ecografia) dell'utero. La diagnosi definitiva e di certezza richiede l'effettuazione di un esame istopatologico. Il quadro ecografico della mola idatiforme ricorda nell'aspetto un grappolo d'uva (si parla anche di aspetto di "utero a nido d'ape" o utero con "tempesta di neve".[4][28][29] Il trofoblasto prolifera molto più del normale e vi è un marcato ampliamento dei villi coriali. L'angiogenesi nei trofoblasti appare gravemente compromessa.
Trattamento
modificaLa mola idatiforme deve essere trattata con la completa rimozione dall'utero mediante la sua aspirazione uterina (isterosuzione) oppure ricorrendo al curettage chirurgico il più presto possibile dopo la diagnosi, al fine di evitare i rischi di evoluzione in coriocarcinoma.[30] Le pazienti sono seguite fino a quando la concentrazione ematica di gonadotropina corionica (hCG) non raggiunge un livello così basso da divenire non più rilevabile. Le mole invasive o metastatiche (tumore) possono richiedere l'esecuzione della chemioterapia specifica e spesso rispondono bene al metotrexate. Dal momento che contengono antigeni paterni, la risposta al trattamento è quasi del 100%. Le pazienti sono invitate a non concepire per un anno, dopo aver sviluppato una gravidanza molare.
L'intervento di raschiamento uterino è generalmente fatto sotto l'effetto dell'anestesia spinale e preferibilmente in pazienti emodinamicamente stabili. I vantaggi dell'anestesia spinale sono rappresentati dalla tecnica relativamente facile, dagli effetti polmonari e respiratori favorevoli, dalla possibilità di essere utilizzata con sicurezza nelle pazienti che presentano segni di ipertiroidismo, ed infine dalle proprietà farmacologiche non tocolitiche.
Inoltre, dal momento che la paziente resta cosciente, è più facile diagnosticare eventuali complicanze, come la perforazione uterina, il distress cardiopolmonare e la tempesta tiroidea in una fase precoce rispetto a quanto avviene quando la paziente è sedato o sotto anestesia generale.[31][32]
La gestione è decisamente più complicata quando la mola si verifica associata alla presenza in utero di uno o più feti normali. Carboprost (PGF2α) è un farmaco che può essere utilizzato per determinare la contrazione uterina.
Prognosi
modificaPiù dell'80% delle mole idatiforme sono benigne. Il risultato che si ottiene dopo il trattamento è di solito eccellente.
Un follow-up frequente è essenziale. Le donne debbono adottare un metodo contraccettivo molto efficace e viene raccomandato loro di evitare la gravidanza per almeno 6 mesi o meglio per 1 anno.
Nel 10-15% dei casi la mola idatiforme può svilupparsi in una forma di mola estremamente invasiva.
Questa condizione prende il nome di malattia trofoblastica persistente (PTD).
Le mole possono infiltrarsi così profondamente nella parete uterina che ne può conseguire una grave emorragia oppure altre complicanze. Questo è il motivo per cui, una volta completato l'intervento chirurgico, i medici tendono a richiedere l'esecuzione di una radiografia addominale completa e di una radiografia del torace.
Nel 2-3% dei casi, una mola idatiforme può svilupparsi in coriocarcinoma, una forma di tumore maligno, caratterizzato da una rapida crescita e dalla tendenza a diffondere (metastatizzare) con facilità.
Nonostante queste caratteristiche, che normalmente depongono per una prognosi sfavorevole, la percentuale di guarigione, dopo un adeguato trattamento chemioterapico, è alta.
Oltre il 90% delle donne affette da tumore maligno, non metastatizzato, sono in grado di sopravvivere e di mantenere la loro capacità di concepire e avere figli.
Nelle donne con cancro e metastasi, la percentuale di remissione si attesta comunque tra il 75 e l'85%, anche se, di norma, viene persa irreversibilmente la capacità di concepire.
La prognosi della mola idatiforme può essere stimata ricorrendo ad un sistema di punteggio, come ad esempio il Modified WHO Prognostic Scoring System, nel quale si sommano punteggi variabili da 1 a 4 tenendo in considerazione diversi parametri.[33]
| 0 | 1 | 2 | 4 | |
|---|---|---|---|---|
| Età | <40 | ≥40 | – | – |
| Gravidanze precedenti | mola | aborto | a termine | – |
| Intervallo (in mesi) dalla gravidanza indice | <4 | 4–6 | 7–12 | >12 |
| hCG sierica pretrattamento (IU/L) | <103 | 103–104 | 104–105 | >105 |
| Dimensioni del tumore (incluso l'utero) | <3 | 3–4 cm | ≥5 cm | – |
| Localizzazione delle metastasi | polmone | milza, rene | gastrointestinali | fegato, cervello |
| Numero di metastasi | – | 1–4 | 5–8 | >8 |
| Precedente chemioterapia fallita | – | – | singolo farmaco | ≥2 farmaci |
Le donne con un punteggio pari o superiore a 7 debbono essere considerate ad alto rischio.
Note
modifica- ^ Cotran RS, Kumar V, Fausto N, Nelso F, Robbins SL, Abbas AK, Robbins and Cotran pathologic basis of disease, 7th, St. Louis, Mo, Elsevier Saunders, 2005, pp. 1110, ISBN 0-7216-0187-1.
- ^ Pathologic Basis of Disease, 8ª ed., Saunders Elsevier, 2010, pp. 1057–1058, ISBN 1-4377-0792-0.
- ^ Kumar V, Abbas AK, Fausto N, Aster, JC, Pathologic Basis of Disease, 8ª ed., Saunders Elsevier, 2010, pp. 1057–1058, ISBN 1-4377-0792-0.
- ^ a b C. Fine, AL. Bundy; RS. Berkowitz; SB. Boswell; AF. Berezin; PM. Doubilet, Sonographic diagnosis of partial hydatidiform mole., in Obstet Gynecol, vol. 73, 3 Pt 1, marzo 1989, pp. 414-8, PMID 2644599.
- ^ JR. Palmer, Advances in the epidemiology of gestational trophoblastic disease., in J Reprod Med, vol. 39, n. 3, marzo 1994, pp. 155-62, PMID 8035370.
- ^ E. Di Cintio, F. Parazzini; C. Rosa; L. Chatenoud; G. Benzi, The epidemiology of gestational trophoblastic disease., in Gen Diagn Pathol, vol. 143, n. 2-3, novembre 1997, pp. 103-8, PMID 9443567.
- ^ BW. Tham, JE. Everard; JA. Tidy; D. Drew; BW. Hancock, Gestational trophoblastic disease in the Asian population of Northern England and North Wales., in BJOG, vol. 110, n. 6, Giu 2003, pp. 555-9, PMID 12798471.
- ^ PC. Lorigan, S. Sharma; N. Bright; RE. Coleman; BW. Hancock, Characteristics of women with recurrent molar pregnancies., in Gynecol Oncol, vol. 78, 3 Pt 1, Set 2000, pp. 288-92, DOI:10.1006/gyno.2000.5871, PMID 10985882.
- ^ NJ. Sebire, RA. Fisher; M. Foskett; H. Rees; MJ. Seckl; ES. Newlands, Risk of recurrent hydatidiform mole and subsequent pregnancy outcome following complete or partial hydatidiform molar pregnancy., in BJOG, vol. 110, n. 1, gennaio 2003, pp. 22-6, PMID 12504931.
- ^ a b MK. Kokanali, D. Oztürkkan; N. Unsal; P. Möroy; T. Güngör; L. Mollamahmutoğlu, Plasma homocysteine, vitamin B12 and folate levels in hydatidiform moles and histopathological subtypes., in Arch Gynecol Obstet, vol. 278, n. 6, Dic 2008, pp. 531-4, DOI:10.1007/s00404-008-0637-0, PMID 18379803.
- ^ M. Harma, M. Harma; A. Kocyigit; S. Yurtseven; N. Demir, Serum levels of folate, vitamin B12 and homocysteine in complete hydatidiform mole., in J Reprod Med, vol. 49, n. 4, aprile 2004, pp. 285-8, PMID 15134154.
- ^ RS. Berkowitz, DW. Cramer; MR. Bernstein; S. Cassells; SG. Driscoll; DP. Goldstein, Risk factors for complete molar pregnancy from a case-control study., in Am J Obstet Gynecol, vol. 152, n. 8, Ago 1985, pp. 1016-20, PMID 4025447.
- ^ K. Ito, [Morphological investigation in microscopic mole]., in Nihon Sanka Fujinka Gakkai Zasshi, vol. 44, n. 7, Lug 1992, pp. 853-8, PMID 1500807.
- ^ DR. Genest, Partial hydatidiform mole: clinicopathological features, differential diagnosis, ploidy and molecular studies, and gold standards for diagnosis., in Int J Gynecol Pathol, vol. 20, n. 4, Ott 2001, pp. 315-22, PMID 11603213.
- ^ NJ. Sebire, M. Foskett; FJ. Paradinas; RA. Fisher; RJ. Francis; D. Short; ES. Newlands; MJ. Seckl, Outcome of twin pregnancies with complete hydatidiform mole and healthy co-twin., in Lancet, vol. 359, n. 9324, Giu 2002, pp. 2165-6, DOI:10.1016/S0140-6736(02)09085-2, PMID 12090984.
- ^ A. Paoloni-Giacobino, Epigenetics in reproductive medicine., in Pediatr Res, vol. 61, 5 Pt 2, Mag 2007, pp. 51R-57R, DOI:10.1203/pdr.0b013e318039d978, PMID 17413849.
- ^ DC. Wallace, U. Surti; CW. Adams; AE. Szulman, Complete moles have paternal chromosomes but maternal mitochondrial DNA., in Hum Genet, vol. 61, n. 2, 1982, pp. 145-7, PMID 6290372.
- ^ L. Sundvall, H. Lund; I. Niemann; UB. Jensen; L. Bolund; L. Sunde, Tetraploidy in hydatidiform moles., in Hum Reprod, vol. 28, n. 7, Lug 2013, pp. 2010-20, DOI:10.1093/humrep/det132, PMID 23633551.
- ^ SD. Lawler, RA. Fisher; J. Dent, A prospective genetic study of complete and partial hydatidiform moles., in Am J Obstet Gynecol, vol. 164, 5 Pt 1, Mag 1991, pp. 1270-7, PMID 1674641.
- ^ R. Slim, A. Mehio, The genetics of hydatidiform moles: new lights on an ancient disease., in Clin Genet, vol. 71, n. 1, gennaio 2007, pp. 25-34, DOI:10.1111/j.1399-0004.2006.00697.x, PMID 17204043.
- ^ C. Deveault, JH. Qian; W. Chebaro; A. Ao; L. Gilbert; A. Mehio; R. Khan; SL. Tan; A. Wischmeijer; P. Coullin; X. Xie, NLRP7 mutations in women with diploid androgenetic and triploid moles: a proposed mechanism for mole formation., in Hum Mol Genet, vol. 18, n. 5, marzo 2009, pp. 888-97, DOI:10.1093/hmg/ddn418, PMID 19066229.
- ^ L. Schwentner, W. Schmitt; G. Bartusek; R. Kreienberg; D. Herr, Cervical hydatidiform mole pregnancy after missed abortion presenting with severe vaginal bleeding: case report and review of the literature., in Eur J Obstet Gynecol Reprod Biol, vol. 156, n. 1, Mag 2011, pp. 9-11, DOI:10.1016/j.ejogrb.2010.12.029, PMID 21272989.
- ^ DJ. Beless, Cervical hydatidiform mole causing severe vaginal hemorrhage: a case report., in J Reprod Med, vol. 40, n. 12, Dic 1995, pp. 855-8, PMID 8926616.
- ^ Ganong WF, McPhee SJ, Lingappa VR, Pathophysiology of Disease: An Introduction to Clinical Medicine (Lange), McGraw-Hill Medical, 2005, pp. 639, ISBN 0-07-144159-X.
- ^ JM. Hershman, Human chorionic gonadotropin and the thyroid: hyperemesis gravidarum and trophoblastic tumors., in Thyroid, vol. 9, n. 7, Lug 1999, pp. 653-7, PMID 10447009.
- ^ M. Yoshimura, JM. Hershman, Thyrotropic action of human chorionic gonadotropin., in Thyroid, vol. 5, n. 5, Ott 1995, pp. 425-34, PMID 8563483.
- ^ JM. Hershman, Physiological and pathological aspects of the effect of human chorionic gonadotropin on the thyroid., in Best Pract Res Clin Endocrinol Metab, vol. 18, n. 2, Giu 2004, pp. 249-65, DOI:10.1016/j.beem.2004.03.010, PMID 15157839.
- ^ JS. Woo, C. Hsu; LL. Fung; HK. Ma, Partial hydatidiform mole: ultrasonographic features., in Aust N Z J Obstet Gynaecol, vol. 23, n. 2, Mag 1983, pp. 103-7, PMID 6578773.
- ^ P. Naumoff, AE. Szulman; B. Weinstein; J. Mazer; U. Surti, Ultrasonography of partial hydatidiform mole., in Radiology, vol. 140, n. 2, Ago 1981, pp. 467-70, PMID 7255725.
- ^ Cotran RS, Kumar V, Fausto N, Nelso F, Robbins SL, Abbas AK, Robbins and Cotran pathologic basis of disease, 7ª ed., St. Louis, Mo, Elsevier Saunders, 2005, pp. 1112, ISBN 0-7216-0187-1.
- ^ G. Biyani, P. Bhatia, Mortality in hydatidiform mole: Should we blame thyroid?, in Indian J Anaesth, vol. 55, n. 6, novembre 2011, pp. 628-9, DOI:10.4103/0019-5049.90629, PMID 22223914.
- ^ T. Bruun, K. Kristoffersen, Thyroid function during pregnancy with special reference to hydatidiform mole and hyperemesis., in Acta Endocrinol (Copenh), vol. 88, n. 2, Giu 1978, pp. 383-9, PMID 78652.
- ^ a b Stage Information for Gestational Trophoblastic Tumors and Neoplasia at The National Cancer Institute (NCI), part of the National Institutes of Health (NIH), in turn citing: FIGO Committee on Gynecologic Oncology.: Current FIGO staging for cancer of the vagina, fallopian tube, ovary, and gestational trophoblastic neoplasia. Int J Gynaecol Obstet 105 (1): 3-4, 2009
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su mola idatiforme
| Controllo di autorità | Thesaurus BNCF 53320 · LCCN (EN) sh85106289 · BNF (FR) cb12267348j (data) · J9U (EN, HE) 987007533939905171 · NDL (EN, JA) 00563569 |
|---|