Verde di Parigi
Il verde di Parigi è un composto chimico più precisamente denominato acetato arsenito di rame(II); la sua formula è in genere riportata come Cu(C2H3O2)2·3Cu(AsO2)2.[3] È una polvere cristallina di colore verde brillante, molto tossica a causa della presenza di arsenico. Il nome verde di Parigi deriva dal fatto che nell'Ottocento fu usato per derattizzare le fogne di Parigi.[4][5] Il composto è noto anche con oltre 80 diverse denominazioni, tra le quali verde di Schweinfurt e verde smeraldo, e fu ampiamente usato come pigmento nel XIX secolo prima di rendersi conto della sua tossicità.[6][7] In passato è stato usato anche come rodenticida e insetticida;[8] negli anni 1944-45 fu sparso con aeroplani come larvicida per controllare la malaria in Italia, Sardegna e Corsica.[9] Nei fuochi artificiali dà un colore blu.[10] Dagli anni 60 del secolo scorso non è più commercializzato come pigmento per artisti.[11] A partire dal 2015, ne è vietato l'uso come agente antivegetativo, come conservante del legno e per il trattamento dell'acqua.[3]
| Verde di Parigi | |
|---|---|
 | |
| Nome IUPAC | |
| Bis(acetato)esametaarsenitotetrarame | |
| Nomi alternativi | |
| Rame acetoarsenito, verde di Basilea, verde di Lipsia, verde di Schweinfurt, verde di Vienna, verde smeraldo, verde pappagallo, verde imperiale, verde nuovo, verde persiano, verde Mitis, verde reale, verde patentato, C.I. 77410 (pigmento verde 21)[1][2] | |
| Caratteristiche generali | |
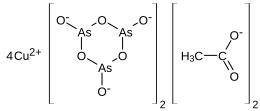
| Formula bruta o molecolare | Cu(C2H3O2)2·3Cu(AsO2)2 |
| Massa molecolare (u) | 1013,80 |
| Aspetto | polvere cristallina verde smeraldo |
| Numero CAS | |
| Numero EINECS | 601-658-7 |
| PubChem | 22833492 |
| SMILES | CC(=O)[O-].CC(=O)[O-].[O-][As]=O.[O-][As]=O.[O-][As]=O.[O-][As]=O.[O-][As]=O.[O-][As]=O.[Cu+2].[Cu+2].[Cu+2].[Cu+2] |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | leggermente solubile[3] |
| Temperatura di fusione | decompone per riscaldamento[3] |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 22 oral rat[3] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 331 - 301 - 410 [3] |
| Verde di Parigi | |
|---|---|
| Coordinate del colore | |
| HEX | #50C878 |
| sRGB1 (r; g; b) | (80; 200; 120) |
| CMYK2 (c; m; y; k) | (60; 0; 40; 22) |
| HSV (h; s; v) | (140°; 60%; 78%) |
| 1: normalizzato a [0-255] (byte) 2: normalizzato a [0-100] (%) | |
Storia
modificaNon è chiaro chi sia stato il primo a preparare questo pigmento, che fu sviluppato con l'intento di migliorare le caratteristiche del verde di Scheele (chimicamente un arsenito di rame). È certo che Wilhelm Sattler (1784-1859) e Friedrich Ruß commercializzarono nel 1814 un pigmento chiamato verde di Schweinfurt (dal nome della città di Schweinfurt), mentre Ignaz von Mitis (1771-1842) produsse lo stesso composto a Vienna, sempre nel 1814.[7] Questo rende ragione dei nomi verde di Mitis e verde di Vienna usati per indicare lo stesso composto. Inizialmente i fabbricanti mantennero segreto il metodo di preparazione, finché nel 1822 il chimico tedesco Justus von Liebig pubblicò un articolo che descriveva composizione e sintesi del composto.[12] In seguito il pigmento fu sintetizzato diffusamente in varie fabbriche in Europa e negli Stati Uniti, con procedimenti differenti che fornivano diverse sfumature di colore, e fu commercializzato utilizzando più di 80 nomi diversi.[7]
Come colore verde fu utilizzato da molti pittori, specie preraffaeliti e impressionisti. Inizialmente non ci si rese conto della tossicità dell'arsenico contenuto in questo pigmento. Data la sua bellezza fu prodotto su scala industriale e trovò largo impiego anche in oggetti di uso comune tra i quali carta da parati, sapone, giochi per bambini, vestiti e persino decorazioni per dolci. Il chimico tedesco Leopold Gmelin aveva pubblicato già nel 1839 un articolo mettendo in guardia sulla pericolosità della carta da parati contenente pigmenti all'arsenico, suggerendo che l'arsenico potesse liberarsi in seguito a una reazione di fermentazione del materiale organico della carta.[13] L'appello rimase inascoltato. I lavoratori impiegati nella produzione soffrirono di avvelenamento cronico da arsenico. L'uso in pittura non risultò particolarmente pericoloso, a meno che il pittore non leccasse il pennello. L'uso in decorazioni per dolci provocò alcuni decessi, ma anche questo non fu correlato con l'arsenico.[14]
I problemi maggiori derivarono dall'uso del pigmento nelle carte da parati. Molti chimici e medici cominciarono a sospettare che il pigmento verde fosse responsabile di malattie e morti inspiegabili, soprattutto di bambini che dormivano in stanze decorate con queste carte da parati. Tuttavia tutte le analisi ripetutamente effettuate da numerosi ricercatori non evidenziavano arsenico rilasciato nell'aria.[13][15] Come si sarebbe capito in seguito, il composto d'arsenico che si liberava era tossico anche a concentrazioni che a quel tempo non era possibile rivelare. Solo alla fine dell'Ottocento il microbiologo Bartolomeo Gosio dimostrò che il rilascio di gas molto tossici contenenti arsenico era dovuto alla presenza di muffe, e mise a punto un test abbastanza sensibile.[16] L'esatta natura del composto tossico rimase sconosciuta fino al 1933, quando il chimico Frederick Challenger lo identificò come trimetilarsina.[17] Già nel 1874, tuttavia, la Commissione sanitaria dello Stato del Michigan aveva avviato una campagna di sensibilizzazione sulla tossicità della carta da parati contenente arsenico, realizzando allo scopo anche un volume, Shadows from the Walls of Death, che raccoglieva campioni di carta da parati in verde di Parigi e che era consultabile solo utilizzando appositi guanti.[18]
È stato ipotizzato che anche la morte di Napoleone Bonaparte sia collegata ad avvelenamento da carta da parati. Benché questo non si sia potuto dimostrare con certezza, è stato stabilito che la residenza dove soggiornò Napoleone a Sant'Elena aveva pareti decorate con carte da parati contenenti arsenico, e l'analisi dei capelli di Napoleone rivela che alla fine della sua vita era stato esposto a concentrazioni elevate di arsenico.[14]
Sintesi
modificaIl verde di Parigi si può preparare in vari modi. Il modo più comune è fare reagire solfato di rame, triossido di diarsenico, carbonato di sodio e acido acetico:[19]
Galleria d'immagini
modifica-
Confezione di verde di Parigi
-
Miscelazione del verde di Parigi con polvere di strada prima di spargerlo nei luoghi di riproduzione di zanzare durante la seconda guerra mondiale
-
Uso come insetticida, poster pubblicato dal US Public Health Service
Note
modifica- ^ Villavecchia e Eigenmann, p. 2712.
- ^ Pedrini 2007
- ^ a b c d e f GESTIS.
- ^ Wills 2012
- ^ Robin 2014
- ^ Ball 2002
- ^ a b c Eastaugh et al. 2004
- ^ Hackett 1926
- ^ Andrews 1963
- ^ Partin 2015
- ^ Zieske 1995
- ^ Ehrmann 1834
- ^ a b Sanger 1894
- ^ a b Emsley 2005
- ^ Andreas 1996
- ^ Gosio 1892
- ^ Challenger et al. 1933
- ^ Zalewski.
- ^ Richardson 2002
Bibliografia
modifica- (DE) H. Andreas, Schweinfurter Grün – das brillante Gift, in Chemie in unserer Zeit, vol. 30, n. 1, 1996, pp. 23-31, DOI:10.1002/ciuz.19960300105.
- J. M. Andrews, Preventive Medicine in World War II, Malaria, Chapter V. North Africa, Italy, and the Islands of the Mediterranean, su history.amedd.army.mil, U.S. Army Medical Department, 1963. URL consultato il 15 novembre 2015 (archiviato dall'url originale il 9 ottobre 2019).
- P. Ball, Colore. Una biografia, Milano, Rizzoli, 2002, ISBN 88-17-86812-4.
- (EN) F. Challenger, C. Higginbottom e L. Ellis, The formation of organo-metalloidal compounds by microorganisms. Part I. Trimethylarsine and dimethylethylarsine, in J. Chem. Soc., 1933, pp. 95-101, DOI:10.1039/JR9330000095.
- (EN) N. Eastaugh, V. Walsh, T. Chaplin e R. Siddall, The Pigment Compendium. A Dictionary of Historical Pigments, Oxford, Elsevier, 2004, ISBN 0-7506-5749-9.
- (DE) E. Ehrmann, Zusammensetzung des Schweinfurter Grün, in Annalen der Physik und Chemie, vol. 32, 1834, pp. 473-476.
- (EN) J. Emsley, The elements of murder, Oxford, Oxford University Press, 2005, ISBN 0-19-280599-1.
- GESTIS, Copper(II) arsenite acetate, su gestis-en.itrust.de. URL consultato il 31 ottobre 2015. Pagina del Copper(II) arsenite acetate nel data base GESTIS.
- B. Gosio, Azione di alcune muffe sui composti fissi d'arsenico, in Rivista d'Igiene e Sanità Pubblica, vol. 3, 1892, pp. 201-30.
- L. W. Hackett, Importanza ed usi del verde di Parigi (aceto-arsenito di rame) per la lotta contro le larve di Anopheles, in Rivista di malariologia, vol. 5, 1926, p. 59.
- L. Partin, Copper as a Colorant, su skylighter.com, Skylighter, 2015. URL consultato il 10 novembre 2015.
- M. Pedrini, Verde di Schweinfurt, su Il pigmento, materia prima di ogni arte pittorica, Sebino Colori, 2007. URL consultato il 10 novembre 2015 (archiviato dall'url originale il 17 novembre 2015).
- (EN) H. W. Richardson, Copper compounds, in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, 2002, DOI:10.1002/14356007.a07_567.
- (EN) M.-M. Robin, Our Daily Poison: From Pesticides to Packaging, How Chemicals Have Contaminated the Food Chain and Are Making Us Sick, New York, New Press, 2014, ISBN 978-1-59558-930-9.
- (EN) C. R. Sanger, On the formation of volatile compounds of arsenic from arsenical wall papers, in Proceedings of the American Academy of Arts and Sciences, vol. 29, 1894, pp. 112-147, DOI:10.2307/20020553.
- G. V. Villavecchia e G. Eigenmann, Rame acetoarsenito, in Nuovo dizionario di merceologia e chimica applicata, vol. 6, Hoepli, 1976, ISBN 88-203-1045-7.
- (EN) J. Wills, US Environmental History: Inviting Doomsday, Edinburgh University Press, 2012, ISBN 0-7486-7236-2.
- (EN) Alexander J. Zawacki, How a Library Handles a Rare and Deadly Book of Wallpaper Samples, in Atlas Obscura, 23 gennaio 2018. URL consultato il 12 novembre 2019.
- F. Zieske, An Investigation of Paul Cézanne's Watercolors With Emphasis on Emerald Green, su cool.conservation-us.org, 1995. URL consultato il 15 novembre 2015.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su Verde di Parigi